
| A. | SO2、SO3都是极性分子 | |
| B. | 元素电负性越大的原子,吸引电子能力越强 | |
| C. | 非极性键可以存在于化合物中 | |
| D. | 离子化合物的熔点不一定比共价化合物的高 |
分析 A.一般情况下中心原子上的价电子都形成共价键的分子为非极性分子,存在孤电子对的分子为极性分子;
B.非金属性越强,电负性越大,该元素的原子吸引电子的能力越强;
C.同种非金属元素之间形成非极性共价键;
D.共价化合物为原子晶体时熔点较高.
解答 解:A.SO2存在孤电子对为极性分子,SO3中心原子上的价电子都形成共价键的分子为非极性分子,故A错误;
B.非金属性越强,电负性越大,该元素的原子吸引电子的能力越强,故B正确;
C.过氧化氢中存在氧元素和氢元素形成的极性共价键,也存在氧元素和氧元素形成的非极性共价键,故C正确;
D.离子化合物的熔点不一定比共价化合物的熔点高,如二氧化硅为原子晶体,其熔点大于NaCl的熔点(离子晶体),故D正确;
故选A.
点评 本题考查了分子极性的判断,电负性,原子晶体的性质等,题目考查知识点较多,但是较基础.


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中只能含离子键,不能有共价键 | |
| B. | 非金属元素之间形成的化学键一定是共价键 | |
| C. | 电子数相同的两种微粒一定是同一元素 | |
| D. | 化学键被破坏的变化不一定是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有羟基的有机物称为醇 | |
| B. | 能发生银镜反应的有机物都是醛 | |
| C. | 苯酚俗称石炭酸,酸性比碳酸强 | |
| D. | 含较多饱和脂肪酸成分的甘油酯一般呈固态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C60气化和金刚石熔化克服的作用力相同 | |
| B. | 甲酸甲酯的熔点低于乙酸的熔点 | |
| C. | 氯化钠和氯化氢溶于水时,破坏的化学键都是离子键 | |
| D. | 分子晶体的熔沸点低,常温下均呈液态或气态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸钠固体 | B. | 硫酸铜固体 | C. | 硝酸钾溶液 | D. | 氯化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
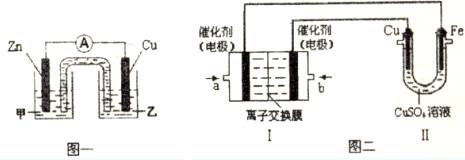
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com