
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+,取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀.由此可知原溶液中
A.至少存在5种离子
B.Cl-一定存在,且c(Cl?)≥0.4mol/L
C.SO42-、NH4+、一定存在,Cl-可能不存在
D.CO32-、Al3+一定不存在,K+可能存在
B
【解析】由于加入过量NaOH溶液,加热,得到0.02mol气体,说明一定有NH4+,且物质的量为0.02mol;同时产生红褐色沉淀,说明一定有Fe3+,1.6g固体为氧化铁,物质的量为0.01mol,故有0.02molFe3+,一定没有CO32-;4.66g不溶于盐酸的沉淀为硫酸钡,一定有SO42-,物质的量为0.02mol;根据电荷守恒,一定有Cl-,至少0.02mol×3+0.02-0.02mol×2=0.04mol,物质的量浓度至少 0.04mol/L。A、至少存在Cl-、SO42-、NH4+、Fe3+四种离子,故A错误; B、根据电荷守恒,至少存在0.04molCl-,故B正确; C、一定存在氯离子,故C错误; D、Al3+无法判断是否存在,故D错误;答案选B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014高考名师推荐化学选做题练习2(解析版) 题型:填空题
氮化硼(BN)是一种重要的功能陶瓷材料.以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示

请回答下列问题:
(1)由B2O3制备BF3、BN的化学方程式依次是 、 ;
(2)基态B原子的电子排布式为 ;B和N相比,电负性较大的是
,BN中B元素的化合价为 ;
(3)在BF3分子中,F-B-F的键角是 ,B原子的杂化轨道类型为
,BF3和过量NaF作用可生成NaBF4,BF4-的立体结构为 ;
(4)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为 ,层间作用力为 ;
(5)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm,立方氮化硼晶胞中含有 个氮原子、 个硼原子,立方氮化硼的密度是 g?cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学离子方程式的书写及正误判断(解析版) 题型:选择题
下列反应的离子方程式书写正确的是
A.等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:Ba2++2OH-+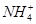 +
+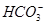 =BaCO3↓+NH3·H2O+H2O
=BaCO3↓+NH3·H2O+H2O
B.氢氧化铁溶于氢碘酸溶液:Fe(OH)3+3H+=Fe3++3H2O
C.向亚硫酸钠溶液中加入足量硝酸: +2H+=SO2↑+H2O
+2H+=SO2↑+H2O
D.向AgNO3溶液中加入过量的氨水:Ag++NH3·H2O=AgOH↓+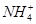
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学离子方程式正误判断(解析版) 题型:选择题
能正确表示下列反应的离子方程式是
A.硫酸铝溶液中加入过量氨水 Al3++3OH-= Al(OH)3↓
B.碳酸钠溶液中加入澄清石灰水 Ca(OH)2+CO32-= CaCO3↓+2OH-
C.冷的氢氧化钠溶液中通入氯气 Cl2+2OH-= ClO-+Cl-+H2O
D.稀硫酸中加入铁粉 2Fe+6H+= 2Fe3++3H2↑
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学离子大量共存与推断(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.0. 1mol·L-1NaOH 溶液: K+、Na+、SO42- 、CO32-
B.0. 1mol·L-1Na2CO3溶液: K+、Ba2+、NO3- 、Cl-
C.0. 1mol·L-1FeCl3溶液: K+、NH4+、I-、SCN-
D.c(H+)/c(OH-)= 1×1014的溶液: Ca2+、Na+、ClO-、NO3-
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学离子共存(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.能溶解Al2O3的溶液:Na+、K+、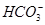 、
、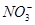
B.0.1 mol·L-1Ca(ClO)2溶液:K+、Na+、I-、Cl-
C.能使甲基橙显红色的溶液:K+、Fe2+、Cl-、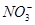
D.加入KSCN显红色的溶液:Na+、Mg2+、Cl-、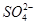
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学碳及其化合物主要性质(解析版) 题型:选择题
下列实验事实所得出的相应结论合理的是
实验事实 | 结论 |
A.Cl2的水溶液可以导电 | Cl2是电解质 |
B.将燃着的镁条伸入盛有CO2的集气瓶中继续燃烧 | 还原性:Mg>C |
C.SO2可以使酸性KMnO4溶液褪色 | SO2具有漂白性 |
D.将铁粉放入稀HNO3中充分反应后,滴入KSCN溶液无明显现象 | 稀HNO3不能将Fe氧化成Fe3+ |
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学盖斯定律及其应用(解析版) 题型:选择题
已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l) △H1
2 H2(g)+ O2(g)= 2H2O(g) △H2
C(s)+ O2(g)=CO2(g) △H3
则反应4C3H5(ONO2)3(l)= 12CO2(g)+10H2O(g) + O2(g) +6N2(g)的△H为
A.12△H3+5△H2-2△H1 B.2△H1-5△H2-12△H3
C.12△H3-5△H2-2△H1 D.△H1-5△H2-12△H3
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学电解三池的应用(解析版) 题型:选择题
某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,原理示意图如下,下列说法不正确的是
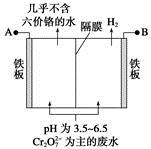
A.A为电源正极
B.阳极区溶液中发生的氧化还原反应为Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
C.阴极区附近溶液pH降低
D.若不考虑气体的溶解,当收集到H213.44 L(标准状况)时,有0.1 mol Cr2O72-被还原
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com