
”¾ĢāÄæ”æÄŖ¶ūŃĪµÄ»ÆѧŹ½ĪŖ( NH4)2Fe(SO4)2”¤6H2O£¬ČÜÓŚĖ®¶ų²»ČÜÓŚŅŅ“¼£¬³£±»ÓĆ×÷Ńõ»Æ»¹ŌµĪ¶ØµÄ»ł×¼Īļ”£ĻĀĆęŹĒÖĘČ”ÄŖ¶ūŃĪµÄ²æ·Ö×°ÖĆÓėŹµŃé²½Öč£ŗ

¢Ł½«ĢśŠ¼·ÅČėŠ”ÉÕ±ÖŠ£¬¼ÓŹŹĮæµÄNa2CO3ČÜŅŗ£¬Š”»š¼ÓČČ¼ø·ÖÖÓ£¬µ¹µōČÜŅŗŗó£¬ÓĆÕōĮóĖ®Ļ“¾»ĢśŠ¼£¬ĮĄøÉ”£
¢ŚŌŚ×¶ŠĪĘæÖŠ¼ÓČė2.24 g ĢśŠ¼ŗĶÉŁĮæĢ¼·Ū£¬ÓÉ·ÖŅŗĀ©¶·µĪ¼Ó20 mL 3 mol/LĮņĖįČÜŅŗ”£
¢Ū“ż·“Ó¦½įŹųŗó£¬ÓÉ·ÖŅŗĀ©¶·¼ÓČėŹŹĮæµÄ(NH4)2SO4ČÜŅŗ£¬¹żĀĖ”£ŌŚĀĖŅŗÖŠ¼ÓČėŅ»¶ØĮæµÄŅŅ“¼£¬“ż¾§ĢåĪö³öŗ󣬹żĀĖ”¢Ļ“µÓ”¢ĮĄøÉ£¬µĆÄŖ¶ūŃĪ¾§Ģ唣
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŹµŃéæŖŹ¼Ē°£¬¼ģ²é·“Ó¦Ę÷ĘųĆÜŠŌµÄ·½·ØĪŖ_____________________”£
£Ø2£©²½Öč¢ŁÖŠNa2CO3ČÜŅŗµÄ×÷ÓĆŹĒ_____________________________________”£
£Ø3£©²½Öč¢ŚÖŠµĪ¼ÓĮņĖįČÜŅŗŹ±ĮōȔɣŠķČÜŅŗÓŚ·ÖŅŗĀ©¶·ÖŠµÄŌŅņŹĒ__________________£¬¼ÓČėÉŁĮæĢ¼·ŪµÄ×÷ÓĆŹĒ_________________________________________”£
£Ø4£©²½Öč¢ŪÖŠĄķĀŪÉĻŠč¼ÓČė2 mol/L µÄ(NH4)2SO4ČÜŅŗ______________mL”£
£Ø5£©Č”10.00 gøõĒąĶѳʷ£¬½«ĘäÖŠµÄøõŃõ»ÆĪŖH2CrO4£¬ŌŁ¼ÓČėĮņĖįĖį»Æ£¬²¢Åä³É250mLČÜŅŗ£¬Č”³ö25.00 mLÓĆÅضČĪŖ0.0180 mol/LµÄ(NH4)2Fe(SO4)2±ź×¼ČÜŅŗµĪ¶Ø£¬ÖÕµćŹ±ÓĆČ„±ź×¼Ņŗ20.75 mL”£ŅŃÖŖČõĖįH2CrO4±»»¹ŌĪŖCr3+£¬ŌņµĪ¶ØŹ±·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ_____________________________________”£øĆѳʷ֊øõŌŖĖŲµÄÖŹĮæ·ÖŹżĪŖ______”£
”¾“š°ø”æ ¹Ų±ÕÖ¹Ė®¼Š£¬“ņæŖ·ÖŅŗĀ©¶·»īČūĻņ׶ŠĪĘæÖŠµĪ¼ÓĖ®£¬ČōŅ»¶ĪŹ±¼äŗóĖ®²»ÄܵĪĻĀĄ“£¬Ōņ·“Ó¦Ę÷ĘųĆÜŠŌĮ¼ŗĆ”££Ø»ņ£ŗ¹Ų±Õ·ÖŅŗĀ©¶·»īČū£¬“ņæŖÖ¹Ė®¼Š£¬½«µ¼¹ÜæŚÖĆÓŚĖ®²ŪÖŠŅŗĆęĻĀ£¬Ī¢ČČ׶ŠĪĘ棬Čōµ¼¹ÜæŚÓŠĘųÅŻ²śÉś£¬Ķ£Ö¹¼ÓČČŅ»¶ĪŹ±¼äŗ󣬹ÜæŚµ¹ĪüŠĪ³ÉŅ»¶ĪĖ®Öł£¬Ōņ·“Ó¦Ę÷ĘųĆÜŠŌĮ¼ŗĆ”££© ³żČ„ĢśŠ¼±ķĆęµÄÓĶĪŪ ĘšŅŗ·ā×÷ÓĆ£¬£Ø·ĄÖ¹Fe2+±»Ńõ»Æ£© ÓėĢś”¢Ļ”ĮņĖį¹¹³ÉŌµē³Ų£¬¼Óæģ·“Ó¦ĖŁĀŹ 20 H2CrO4+3Fe2++6H+=Cr3++3Fe3++4H2O 0.65»ņ65%
”¾½āĪö”æ£Ø1£©ŹµŃéæŖŹ¼Ē°£¬¼ģ²é·“Ó¦Ę÷ĘųĆÜŠŌµÄ·½·ØĪŖ£ŗ¹Ų±ÕÖ¹Ė®¼Š£¬“ņæŖ·ÖŅŗĀ©¶·»īČūĻņ׶ŠĪĘæÖŠµĪ¼ÓĖ®£¬ČōŅ»¶ĪŹ±¼äŗóĖ®²»ÄܵĪĻĀĄ“£¬Ōņ·“Ó¦Ę÷ĘųĆÜŠŌĮ¼ŗĆ£»£Ø»ņ£ŗ¹Ų±Õ·ÖŅŗĀ©¶·»īČū£¬“ņæŖÖ¹Ė®¼Š£¬½«µ¼¹ÜæŚÖĆÓŚĖ®²ŪÖŠŅŗĆęĻĀ£¬Ī¢ČČ׶ŠĪĘ棬Čōµ¼¹ÜæŚÓŠĘųÅŻ²śÉś£¬Ķ£Ö¹¼ÓČČŅ»¶ĪŹ±¼äŗ󣬹ÜæŚµ¹ĪüŠĪ³ÉŅ»¶ĪĖ®Öł£¬Ōņ·“Ó¦Ę÷ĘųĆÜŠŌĮ¼ŗĆ£©£»ÕżČ·“š°ø£ŗ¹Ų±ÕÖ¹Ė®¼Š£¬“ņæŖ·ÖŅŗĀ©¶·»īČūĻņ׶ŠĪĘæÖŠµĪ¼ÓĖ®£¬ČōŅ»¶ĪŹ±¼äŗóĖ®²»ÄܵĪĻĀĄ“£¬Ōņ·“Ó¦Ę÷ĘųĆÜŠŌĮ¼ŗĆ”££Ø»ņ£ŗ¹Ų±Õ·ÖŅŗĀ©¶·»īČū£¬“ņæŖÖ¹Ė®¼Š£¬½«µ¼¹ÜæŚÖĆÓŚĖ®²ŪÖŠŅŗĆęĻĀ£¬Ī¢ČČ׶ŠĪĘ棬Čōµ¼¹ÜæŚÓŠĘųÅŻ²śÉś£¬Ķ£Ö¹¼ÓČČŅ»¶ĪŹ±¼äŗ󣬹ÜæŚµ¹ĪüŠĪ³ÉŅ»¶ĪĖ®Öł£¬Ōņ·“Ó¦Ę÷ĘųĆÜŠŌĮ¼ŗĆ£©”£
£Ø2£©Na2CO3ČÜŅŗĖ®½āĻŌ¼īŠŌ£¬Äܹ»ÓėÓĶĪŪ·¢Éś·“Ó¦£¬æÉŅŌĻ“µÓĢś·ŪÖŠµÄÓĶĪŪ£»ÕżČ·“š°ø£ŗ³żČ„ĢśŠ¼±ķĆęµÄÓĶĪŪ”£
£Ø3£©²½Öč¢ŚÖŠµĪ¼ÓĮņĖįČÜŅŗŹ±ĮōȔɣŠķČÜŅŗÓŚ·ÖŅŗĀ©¶·ÖŠ£¬Äܹ»Ęšµ½Ņŗ·ā×÷ÓĆ£¬·ĄÖ¹æÕĘų°ŃFe2+Ńõ»Æ£»Ģś”¢Ģ¼ŗĶĻ”ĮņĖį¹¹³ÉŌµē³Ų£¬¼Óæģ·“Ó¦ĖŁĀŹ£»ÕżČ·“š°ø£ŗĘšŅŗ·ā×÷ÓĆ£¬£Ø·ĄÖ¹Fe2+±»Ńõ»Æ£©£»ÓėĢś”¢Ļ”ĮņĖį¹¹³ÉŌµē³Ų£¬¼Óæģ·“Ó¦ĖŁĀŹ”£
£Ø4£©2.24 g ĢśŠ¼Óė20 mL 3 mol/LĮņĖįČÜŅŗ·“Ó¦£¬ĮņĖį¹żĮ棬ĻūŗÄĢśµÄĮæĪŖ0.04mol£¬Éś³ÉĮņĖįŃĒĢśµÄĮæĪŖ0.04 mol£¬Č»ŗóøł¾Ż(NH4)2SO4+FeSO4+6H2O =( NH4)2Fe(SO4)2”¤6H2O·“Ó¦æÉÖŖĻūŗÄn(NH4)2SO4)=0.04 mol, øł¾Żc”ĮV=næÉÖŖ£¬0.04=2”ĮV£¬V=0.02L=20 mL£»ÕżČ·“š°ø£ŗ20”£
£Ø5£©øł¾ŻĢāøųŠÅĻ¢æÉÖŖ£¬H2CrO4Äܹ»°Ń(NH4)2Fe(SO4)2ÖŠµÄŃĒĢśĄė×ÓŃõ»ÆĪŖĢśĄė×Ó£¬±¾Éķ»¹ŌĪŖCr3+£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖH2CrO4+3Fe2++6H+=Cr3++3Fe3++4H2O£» øł¾Ż·“Ó¦¹ŲĻµ£ŗH2CrO4-3Fe2+æÉÖŖ£ŗ25.00 mLČÜŅŗÖŠn((NH4)2Fe(SO4)2)=n(Fe2+)=0.018”Į20.75”Į10-3=3.735”Į10-4mol, n( H2CrO4)=1.245”Į10-4mol,Ōņ250mLČÜŅŗŗ¬ÓŠn( H2CrO4)=1.245”Į10-3 mol£»m(Cr)= 1.245”Į10-3”Į52g; øĆѳʷ֊øõŌŖĖŲµÄÖŹĮæ·ÖŹżĪŖ1.245”Į10-3”Į52/10”Į100%=65%£»ÕżČ·“š°ø£ŗH2CrO4+3Fe2++6H+=Cr3++3Fe3++4H2O£»65%»ņ0.65



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijŠĀŠĶÓŠ»śõ£°·»ÆŗĻĪļMŌŚlŅµÉś²śÖŠÓŠÖŲŅŖµÄ×÷ÓĆ£¬ĘäŗĻ³ÉĀ·ĻßČēĻĀ£ŗ

ŅŃÖŖ£ŗ¢ŁAŹĒĢžµÄŗ¬ŃõŃÜÉśĪļ£¬Ļą¶Ō·Ö×ÓÖŹĮæĪŖ58£¬Ģ¼ŗĶĒāµÄÖŹĮæ·ÖŹżÖ®ŗĶĪŖ44.8%£¬ŗĖ“Ź²ÕńĒāĘ×ĻŌŹ¾ĪŖŅ»×é·å£¬æÉ·¢ÉśŅų¾µ·“Ó¦”£
¢Ś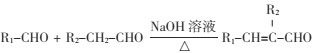
¢Ū![]()
¢Ü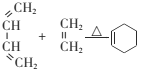
»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)EµÄ½į¹¹¼ņŹ½ĪŖ ___£¬GµÄĆū³ĘĪŖ_____
(2)BÖŠŗ¬ÓŠ¹ŁÄÜĶŵÄĆū³ĘĪŖ_______”£
(3)C-DµÄ·“Ó¦ĄąŠĶĪŖ ___”£
(4)Š“³ö F+H”ŖMµÄ»Æѧ·“Ó¦·½³ĢŹ½____”£
(5)·¼Ļć×å»ÆŗĻĪļWÓŠČżøöČ”“ś»ł£¬ŹĒCµÄĶ¬·ÖŅģ¹¹Ģ壬ÄÜÓėFeCl3ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦”£ 0.5 molWæÉÓė×ćĮæµÄNa·“Ӧɜ³É1gH2£¬HŗĖ“Ź²ÕńĒāĘ×ĻŌŹ¾ĪŖĪå×é·å£¬·ūŗĻŅŌÉĻĢõ¼žµÄWµÄĶ¬·ÖŅģ¹¹Ģå¹²ÓŠ___ ÖÖ£¬Š“³öĘäÖŠŅ»ÖֵĽį¹¹¼ņŹ½____”£
(6)²ĪÕÕÉĻŹöŗĻ³ÉĀ·Ļߣ®ŅŌCH2=CH2ŗĶHOCH2CH2OHĪŖŌĮĻ£ØĪŽ»śŹŌ¼ĮČĪŃ”£©£¬Éč¼ĘÖʱø![]() µÄŗĻ³ÉĀ·Ļß________”£
µÄŗĻ³ÉĀ·Ļß________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲŹµŃéµÄ²Ł×÷²»ÕżČ·µÄŹĒ£Ø £©
A.·ÖŅŗŹ±£¬·ÖŅŗĀ©¶·ÄŚµÄÉĻ²ćŅŗĢåÓ¦ÓÉÉĻæŚµ¹³ö
B.ÓĆ¼ÓČČ·Ö½āµÄ·½·ØĒų·ÖĢ¼ĖįÄĘŗĶĀČ»ÆÄĘĮ½ÖÖ¹ĢĢå
C.¹żĀĖĒāŃõ»ÆÄĘČÜŅŗ³żČ„²»ČÜŠŌŌÓÖŹŹ±£¬ŠčÓĆ²£Į§°ōŅżĮ÷
D.ijČÜŅŗÖŠ¼ÓČėĻõĖįĖį»ÆµÄĻõĖįŅųČÜŅŗ£¬²śÉś°×É«³Įµķ£¬øĆČÜŅŗÖŠŗ¬ÓŠĀČĄė×Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹Ųµē½āÖŹµÄĖµ·ØÕżČ·µÄŹĒ£Ø £©
A.Ēæµē½āÖŹµÄČÜŅŗŅ»¶Ø±ČČõµē½āÖŹµÄČÜŅŗµ¼µēŠŌĒæ
B.Ēæµē½āÖŹµÄČÜŅŗÖŠÖ»ÓŠŅõ”¢ŃōĄė×Ó
C.Ąė×Ó»ÆŗĻĪļ¶¼ŹĒĒæµē½āÖŹ£¬¶ųČõµē½āÖŹ¶¼ŹĒ¹²¼Ū»ÆŗĻĪļ
D.ÓÉÓŚĮņĖį±µÄŃČÜÓŚĖ®£¬ĖłŅŌŹĒČõµē½āÖŹ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æO2ŗĶO3ŹĒŃõŌŖĖŲµÄĮ½ÖÖµ„ÖŹ£¬øł¾ŻĘä·Ö×ÓŹ½Ķź³ÉĻĀĮŠø÷Ģā£ŗ
£Ø1£©µČÖŹĮæµÄO2ŗĶO3Ėłŗ¬·Ö×ÓøöŹż±ČĪŖ £¬ Ō×ÓøöŹż±ČĪŖ £¬ ·Ö×ÓµÄĪļÖŹµÄĮæÖ®±ČĪŖ £®
£Ø2£©µČĪĀµČŃ¹ĻĀ£¬µČĢå»żµÄO2ŗĶO3Ėłŗ¬·Ö×ÓøöŹż±ČĪŖ £¬ Ō×ÓøöŹż±ČĪŖ £¬ ÖŹĮæ±ČĪŖ £®
£Ø3£©ÉčNAĪŖ°¢·üŁ¤µĀĀŽ³£ŹżµÄŹżÖµ£¬Čē¹ūa gijĘųĢåÖŠŗ¬ÓŠµÄ·Ö×ÓŹżĪŖb£¬Ōņc gøĆĘųĢåŌŚ±ź×¼×“æöĻĀµÄĢå»żŌ¼ŹĒ £ØÓĆŗ¬NAµÄŹ½×Ó±ķŹ¾£©£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŖĮĖ³żČ„“ÖŃĪÖŠµÄCa2+”¢Mg2+”¢SO42-¼°ÄąÉ³£¬æɽ«“ÖŃĪČÜÓŚĖ®£¬Č»ŗó½ųŠŠĻĀĮŠĪåĻī²Ł×÷£ŗ¢Ł¹żĀĖ£¬¢Ś¼Ó ¹żĮæNaOHČÜŅŗ£¬¢Ū¼ÓŹŹĮæŃĪĖį£¬¢Ü¼Ó¹żĮæNa2CO3ČÜŅŗ£¬¢Ż¼Ó¹żĮæBaCl2ČÜŅŗ”£ÕżČ·µÄ²Ł×÷Ė³ŠņŹĒ£Ø £©
A.¢Ś¢Ł¢Ü¢Ż¢ŪB.¢Ü¢Ś¢Ż¢Ł¢ŪC.¢Ś¢Ż¢Ü¢Ł¢ŪD.¢Ż¢Ś¢Ł¢Ü¢Ū
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æA”¢B”¢C”¢DĖÄÖÖĪļÖŹÖ®¼äÓŠĶ¼ĖłŹ¾µÄ×Ŗ»Æ¹ŲĻµ£®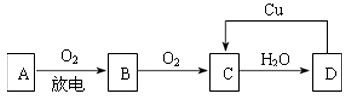
ŅŃÖŖ£¬AŹĒæÕĘųÖŠµÄÖ÷ŅŖ³É·Ö£¬B”¢C”¢D¾łĪŖ»ÆŗĻĪļ£¬ĒŅCĪŖŗģ×ŲÉ«ĘųĢ壮
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
¢ŁŠ“³öAŗĶCµÄ»ÆѧŹ½£ŗA £¬ C £®
¢ŚB”śC¹Ū²ģµ½µÄĻÖĻóŹĒ £®
¢ŪC”śDµÄ»Æѧ·“Ó¦·½³ĢŹ½ŹĒ £¬ øĆ·“Ó¦µÄŃõ»Æ¼ĮŹĒ £¬ »¹Ō¼ĮŹĒ £®
¢ÜŌŚĶ¼Ź¾D”śCµÄ¹ż³ĢÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ £¬ ĘäÖŠ£¬D±ķĻÖ³öĒæ£ØĢī”°Ńõ»ÆŠŌ”±»ņ”°»¹ŌŠŌ”±£©£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ż³Ģ²»Éę¼°»Æѧ±ä»ÆµÄŹĒ
A.ŗ£Ė®É¹ŃĪB.¹āŗĻ×÷ÓĆ
C.øÖĢśÉśŠāD.¾Ę¾«Č¼ÉÕ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄūĆŹĖį(ÓĆHR ±ķŹ¾)ŹĒŅ»ÖÖøߊ§³ż¹ø¼Į£¬ĻÖÓĆŅ»¶ØÅØ¶ČµÄÄūĆŹĖįČÜŅŗČ„³żĖ®¹ø£¬ČÜŅŗÖŠH3R”¢H2R-”¢HR2-”¢R3-µÄŗ¬ĮæĖępHµÄ±ä»ÆČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
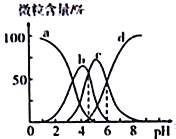
A. H3RµÄµŚ¶ž²½µēĄė³£ŹżKa2(H3R)µÄŹżĮ漶ĪŖ10-4
B. pH=6Ź±£¬c(R3-)=c(HR2-)>c(H+)>c(OH-)
C. Na2HRČÜŅŗÖŠHR2-µÄĖ®½ā³Ģ¶Č“óÓŚµēĄė³Ģ¶Č
D. pH=4Ź±£¬c(H+)=c(H2R-)+2c(HR2-)+c(OH-)
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com