
【题目】一种新型锂-空气电池其工作原理如图所示。放电时,O2与Li+在多孔碳材料电极处生成Li2O2-x(x=0或1)。下列说法正确的是
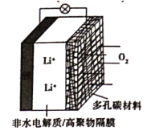
A.锂电极为正极
B.外电路电子由多孔碳材料电极流向锂电极
C.多孔碳材料的O2失电子转化为O2-
D.电池总反应为2Li+(1-x/2)O2=Li2O2-x
【答案】D
【解析】
由可充电锂-空气电池的图片可知,放电时,O2与Li+在多孔碳材料电极生成Li2O2-x,电池总反应为2Li+ (1-![]() )O2=Li2O2-x,因而锂电极为负极,多孔碳材料为正极,根据以上分析进行解答。
)O2=Li2O2-x,因而锂电极为负极,多孔碳材料为正极,根据以上分析进行解答。
A. 由可充电锂-空气电池的图片可知,放电时,O2与Li+在多孔碳材料电极生成Li2O2-x,因而锂电极为负极,多孔碳材料为正极,A项错误;
B. 可充电锂-空气电池的工作原理为原电池的工作原理,放电时,锂电极为负极,外电路电子由锂电极经过导线流向正极,B项错误;
C.由于多孔碳材料电极为正极,得电子发生还原反应,故O2得电子转化为O2-,C项错误;
D. 电池总反应为2Li+ (1-![]() )O2=Li2O2-x,D项正确;
)O2=Li2O2-x,D项正确;
答案选D。


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
【题目】将Mg、Al组成的mg混合物投入一定量稀HCl中,固体完全溶解,收集到气体为1.12L(标准状况),向反应后溶液中加入2 mol/L NaOH溶液60mL时,金属离子恰好沉淀完全,则形成沉淀的质量为( )
A.(m+1.7)gB.(m+2.04)gC.(m+3.4)gD.(m+4.08)g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1mol某烃在氧气中充分燃烧生成CO2和H2O,需要消耗标准状况下的氧气179.2L。它在光照的条件下与氯气反应能生成三种不同的一氯取代物。该烃的结构简式是
A.CH3CH2CH2CH2CH3B.![]()
C.![]() D.
D.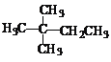
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
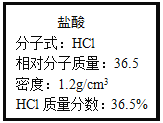
(一)该浓盐酸的物质的量浓度为______mol/L.
(二)某学生欲用上述浓盐酸和蒸馏水配制450mL物质的量浓度为0.3mol/L稀盐酸,可供选用的仪器有:①胶头滴管②烧瓶③烧杯④药匙⑤量筒⑥托盘天平⑦玻璃棒 ,请回答下列问题:
(1)配制稀盐酸时,上述仪器中不需要使用的有______(选填序号),还缺少的仪器有______(写仪器名称).
(2)下列对容量瓶及其使用方法的描述中正确的是______.
A.容量瓶上标有容积、温度和浓度
B.容量瓶用蒸馏水洗净后,必须烘干
C.容量瓶可用来长期储存溶液
D.使用前要检查容量瓶是否漏水
(3)该学生需要量取______mL上述浓盐酸来配制。
(4)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次)________________________;
A.用30mL水洗涤烧杯2--3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量水(约30mL)的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1-2cm处
(5)在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏高”或“偏低”或“无影响”).
I、用量筒量取浓盐酸时俯视观察凹液面______
II、用量筒量取浓盐酸后,洗涤量筒2--3次,洗涤液也转移到容量瓶______
III、溶液注入容量瓶前没有恢复到室温就进行定容______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯度晶体硅是良好的半导体材料,它的发现和使用引起了计算机的一场“革命”。它可以按下列方法制备:
SiO2![]() Si(粗)
Si(粗)![]() SiHCl3
SiHCl3![]() Si(纯)
Si(纯)
下列说法不正确的是( )
A.步骤③中氢气作还原剂
B.硅和二氧化硅都能用作计算机“芯片”
C.步骤①的化学方程式为:SiO2+2C![]() Si+2CO↑
Si+2CO↑
D.步骤①②③中发生的反应都属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法不正确的是
A.9g 13CO2与N217O的混合物中所含中子数目为4.6NA
B.1L 0.1 mol·L-1 Na2CO3溶液中,CO32-离子数小于0.1NA
C.7.1g Cl2与足量NaOH溶液反应转移的电子数为0.2NA
D.14g乙烯中含有的共用电子对数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将标准状况下的HCl气体4.48 L溶于水形成100 mL溶液,然后与足量的铁屑充分反应。计算:
(1)所得盐酸溶液的物质的量浓度_______________
(2)参加反应的铁的质量____________
(3)生成的H2的体积(标况)___________
(4)将生成的FeCl2配成400 mL溶液,此溶液中FeCl2的物质的量浓度____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数,下列叙述中正确的是
A. 标准状况下,22.4 L水中含有的水分子数为NA
B. 1 mol Fe与足量的盐酸反应电子转移总数为3NA
C. 常温常压下,22 g CO2中含有的氧原子数为NA
D. 500 mL 1 mol·L-1MgCl2溶液中含有Cl﹣数目为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度条件下,甲、乙两个容积相等的恒容密闭容器中均发生如下反应:3A(g)+B(g)![]() xC(g)+D(s),向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是( )
xC(g)+D(s),向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是( )
A.平衡时甲中A的体积分数为0.4
B.平衡时甲、乙两容器中A、B的物质的量之比不相等
C.若平衡时两容器中的压强不相等,则两容器中压强之比为8:5
D.若平衡时甲、乙两容器中A的物质的量相等,则x=4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com