
(14·Ö)¹żĢ¼ĖįÄĘ(Na2CO4)ŗĶĻ”ĮņĖį·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2Na2CO4+2H2SO4=2Na2SO4+2CO2”ü+O2”ü+2H2O ij¹żĢ¼ĖįÄĘѳʷ֊ŗ¬ÓŠÉŁĮæ¹żŃõ»ÆÄĘ£¬¼×”¢ŅŅĮ½Ī»Ķ¬Ń§ø÷³ĘȔ֏Įæ ĪŖmµÄøĆѳʷ£¬²¢ÓĆĻĀĶ¼ĖłŹ¾ŹĒŅĒĘ÷²ā¶ØѳʷµÄ“æ¶Č”£ŅĒĘ÷µÄĮ¬½ÓĖ³ŠņŹĒ£ŗ¼×ŹĒ¢Ł¢ß¢Ū¢Ž¢Ü£» ŅŅŹĒ¢Ł¢Ś”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1£©¼×Ķ¬Ń§ĻėĶعżŹµŃé²āµĆµÄŹż¾ŻŹĒ ”£ĖūŹ¹ÓĆÖ®ÖŠ¢Ū______(Ģī”°ÓŠ”±»ņ”°Ć»ÓŠ”±)±ŲŅŖ”£
(2) ŅŅĶ¬Ń§ĻėĶعżŹµŃé²āµĆµÄŹż¾ŻŹĒ ”£°“Ėū²āµĆµÄŹż¾Ż¼ĘĖć³öµÄŹµŃé½į¹ū_______(Ģī ”°Ę«øß”±»ņ”°Ę«µĶ”±)£¬ĄķÓÉŹĒ ”£
(3). ĪŖĮĖ²āµĆ×¼Č·µÄŹµŃ鏿¾Ż£¬ĒėÄć½«ŅŅĶ¬Ń§µÄŹµŃé×°ÖĆ½ųŠŠøĽų(ĆæÖÖŅĒĘ÷Ö»×¼Ź¹ÓĆŅ»“Ī)£¬Š“³öø÷ŅĒĘ÷½ÓµÄĮ¬½ÓĖ³Šņ ”£
(4). °“ÄćÉč¼ĘµÄŹµŃé×°ÖĆ½ųŠŠŹµŃ飬Čō²āµĆŹµŃéĒ°ŗó×°ÖĆ¢ŚµÄÖŹĮæ·Ö±šŹĒw1ŗĶw2£¬Ōņѳʷ֊¹żĢ¼ĖįÄʵÄÖŹĮæ·ÖŹżĪŖ ”£

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
| ĪĀ¶Č”ę Čܽā¶Č ČÜÖŹ g/100gĖ® |
10 | 20 | 30 | 40 | 50 | 60 | 70 |
| NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
| NH4HCO3 | 15.8 | 21.0 | 27.0 | ||||
| NaHCO3 | 8.2 | 9.6 | 11.1 | 12.7 | 14.4 | 16.4 | |
| NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 |
| c”ĮV1 ”Į10-3”ĮM(Na2CO3)g |
| Gg |
| c”ĮV1 ”Į10-3”ĮM(Na2CO3)g |
| Gg |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2011-2012ѧğ°²»ÕŹ”øßČżÉĻѧʌµŚČż“Ī¶Īæ¼»ÆѧŹŌ¾ķ ĢāŠĶ£ŗŹµŃéĢā
(14·Ö)¹żĢ¼ĖįÄĘ(Na2CO4)ŗĶĻ”ĮņĖį·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2Na2CO4+2H2SO4=2Na2SO4+2CO2”ü+O2”ü+2H2O ij¹żĢ¼ĖįÄĘѳʷ֊ŗ¬ÓŠÉŁĮæ¹żŃõ»ÆÄĘ£¬¼×”¢ŅŅĮ½Ī»Ķ¬Ń§ø÷³ĘȔ֏Įæ ĪŖmµÄøĆѳʷ£¬²¢ÓĆĻĀĶ¼ĖłŹ¾ŹĒŅĒĘ÷²ā¶ØѳʷµÄ“æ¶Č”£ŅĒĘ÷µÄĮ¬½ÓĖ³ŠņŹĒ£ŗ¼×ŹĒ¢Ł¢ß¢Ū¢Ž¢Ü£» ŅŅŹĒ¢Ł¢Ś”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
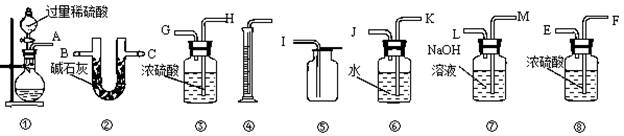
(1£©¼×Ķ¬Ń§ĻėĶعżŹµŃé²āµĆµÄŹż¾ŻŹĒ ”£ĖūŹ¹ÓĆÖ®ÖŠ¢Ū______(Ģī”°ÓŠ”±»ņ”°Ć»ÓŠ”±)±ŲŅŖ”£
(2) ŅŅĶ¬Ń§ĻėĶعżŹµŃé²āµĆµÄŹż¾ŻŹĒ ”£°“Ėū²āµĆµÄŹż¾Ż¼ĘĖć³öµÄŹµŃé½į¹ū_______(Ģī ”°Ę«øß”±»ņ”°Ę«µĶ”±)£¬ĄķÓÉŹĒ ”£
(3). ĪŖĮĖ²āµĆ×¼Č·µÄŹµŃ鏿¾Ż£¬ĒėÄć½«ŅŅĶ¬Ń§µÄŹµŃé×°ÖĆ½ųŠŠøĽų(ĆæÖÖŅĒĘ÷Ö»×¼Ź¹ÓĆŅ»“Ī)£¬Š“³öø÷ŅĒĘ÷½ÓµÄĮ¬½ÓĖ³Šņ ”£
(4). °“ÄćÉč¼ĘµÄŹµŃé×°ÖĆ½ųŠŠŹµŃ飬Čō²āµĆŹµŃéĒ°ŗó×°ÖĆ¢ŚµÄÖŹĮæ·Ö±šŹĒw1ŗĶw2£¬Ōņѳʷ֊¹żĢ¼ĖįÄʵÄÖŹĮæ·ÖŹżĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2012½ģ°²»ÕŹ”ŗĻ·Ź°ĖÖŠøßČżÉĻѧʌµŚČż“Ī¶Īæ¼»ÆѧŹŌ¾ķ ĢāŠĶ£ŗŹµŃéĢā
(14·Ö)¹żĢ¼ĖįÄĘ(Na2CO4)ŗĶĻ”ĮņĖį·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2Na2CO4+2H2SO4=2Na2SO4+2CO2”ü+O2”ü+2H2O ij¹żĢ¼ĖįÄĘѳʷ֊ŗ¬ÓŠÉŁĮæ¹żŃõ»ÆÄĘ£¬¼×”¢ŅŅĮ½Ī»Ķ¬Ń§ø÷³ĘȔ֏Įæ
ij¹żĢ¼ĖįÄĘѳʷ֊ŗ¬ÓŠÉŁĮæ¹żŃõ»ÆÄĘ£¬¼×”¢ŅŅĮ½Ī»Ķ¬Ń§ø÷³ĘȔ֏Įæ ĪŖmµÄøĆѳʷ£¬²¢ÓĆĻĀĶ¼ĖłŹ¾ŹĒŅĒĘ÷²ā¶ØѳʷµÄ“æ¶Č”£ŅĒĘ÷µÄĮ¬½ÓĖ³ŠņŹĒ£ŗ¼×ŹĒ¢Ł¢ß¢Ū¢Ž¢Ü£»ŅŅŹĒ¢Ł¢Ś”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
ĪŖmµÄøĆѳʷ£¬²¢ÓĆĻĀĶ¼ĖłŹ¾ŹĒŅĒĘ÷²ā¶ØѳʷµÄ“æ¶Č”£ŅĒĘ÷µÄĮ¬½ÓĖ³ŠņŹĒ£ŗ¼×ŹĒ¢Ł¢ß¢Ū¢Ž¢Ü£»ŅŅŹĒ¢Ł¢Ś”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ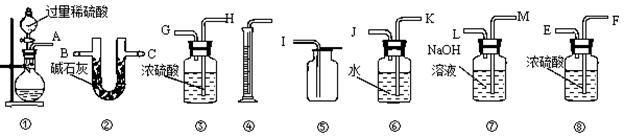
(1£©¼×Ķ¬Ń§ĻėĶعżŹµŃé²āµĆµÄŹż¾ŻŹĒ ”£ĖūŹ¹ÓĆÖ®ÖŠ¢Ū______(Ģī”°ÓŠ”±»ņ”°Ć»ÓŠ”±)±ŲŅŖ”£
(2) ŅŅĶ¬Ń§ĻėĶعżŹµŃé²āµĆµÄŹż¾ŻŹĒ  ”£°“Ėū²āµĆµÄŹż¾Ż¼ĘĖć³öµÄŹµŃé½į¹ū_______(Ģī”°Ę«øß”±»ņ”°Ę«µĶ”±)£¬ĄķÓÉŹĒ ”£
”£°“Ėū²āµĆµÄŹż¾Ż¼ĘĖć³öµÄŹµŃé½į¹ū_______(Ģī”°Ę«øß”±»ņ”°Ę«µĶ”±)£¬ĄķÓÉŹĒ ”£
(3). ĪŖĮĖ²āµĆ×¼Č·µÄŹµŃ鏿¾Ż£¬ĒėÄć½«ŅŅĶ¬Ń§µÄŹµŃé×°ÖĆ½ųŠŠøĽų(ĆæÖÖŅĒĘ÷Ö»×¼Ź¹ÓĆŅ»“Ī)£¬Š“³öø÷ŅĒĘ÷½ÓµÄĮ¬½ÓĖ³Šņ ”£
(4). °“ÄćÉč¼ĘµÄŹµŃé×°ÖĆ½ųŠŠŹµŃ飬Čō²āµĆŹµŃéĒ°ŗó×°ÖĆ¢ŚµÄÖŹĮæ·Ö±šŹĒw1ŗĶw2£¬Ōņѳʷ֊¹żĢ¼ĖįÄʵÄÖŹĮæ·ÖŹżĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com