
| A. | 甲、乙中铝都有剩余 | |
| B. | 铝片的质量是5.4 g | |
| C. | 盐酸或氢氧化钠的物质的量浓度为0.1 mol/L | |
| D. | 盐酸或氢氧化钠的物质的量浓度为0.2 mol/L |
分析 由2Al+6HCl═2AlCl3+3H2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑可知,酸碱足量,生成气体相同;金属足量,酸碱不足,生成气体为1:3,由盐酸和氢氧化钠溶液中溶质的物质的量相同,应结束后测得生成的气体体积比为甲:乙=2:3,比值处于 2:3和1:1之间,由于铝消耗酸量大于碱,此时铝对于酸过量而对于碱不足,结合化学反应方程式计算即可.
解答 解:盐酸和氢氧化钠溶液中溶质的物质的量相等,两烧杯中分别加入铝粉,反应结束后测得生成的气体体积比为甲:乙=2:3,比值处于 2:3和1:1之间,由于铝消耗酸量大于碱,此时铝对于酸过量而对于碱不足;
铝与酸反应时酸完全反应,生成的氢气的物质的量为0.1mol,
则 2Al+6HCl═2AlCl3+3H2↑
2 6 3
$\frac{0.2}{3}$ 0.2 0.1
消耗Al的质量是$\frac{0.2}{3}$mol×27g/mol=1.8g,
碱与金属铝反应时铝完全反应,生成的氢气的物质的量为0.15mol,
则 2Al+2NaOH+2H2O═2NaAlO2+3H2↑
2 2 3
0.1 0.1 0.15mol
则Al的质量为0.1mol×27g/mol=2.7g,
A、甲中铝有剩余,故A错误;
B、甲、乙中消耗铝的质量是1.8g、2.7g,铝对于酸过量而对于碱不足,铝片的质量是5.4g,故B错误;
C、铝对于酸过量而对于碱不足,所以盐酸或氢氧化钠的物质的量浓度为$\frac{0.2mol}{1L}$=0.2 mol/L,故C错误;
D、盐酸或氢氧化钠的物质的量浓度为$\frac{0.2mol}{1L}$=0.2 mol/L,故D正确.
故选D.
点评 本题考查Al的化学性质及利用化学反应方程式的计算,为高频考点,把握铝与酸、碱反应水的化学反应方程式,酸碱足量、酸碱均不足量时得到的氢气的关系是解答本题的关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 78g过氧化钠固体与足量的水反应,转移的电子数目为2NA | |
| B. | Fe在1molCl2中充分燃烧,转移的电子数目为3NA | |
| C. | 将含有0.1molFeCl3的FeCl3饱和溶液,滴入沸水中加热形成Fe(OH)3胶体,所含的胶体粒子数目少于0.1NA | |
| D. | 足量的MnO2粉末与含有4molHCl的浓盐酸充分反应,转移的电子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:D>E>B>A | |
| B. | C和E的单质可通过电解饱和的CE水溶液获得 | |
| C. | C与A形成的两种化合物中化学键类型和晶体类型完全相同 | |
| D. | A、D、E的最高价氧化物对应水化物的酸性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:b>a>c>d | B. | 原子半径:A>B>C>D | ||
| C. | 金属性:B>A,非金属性:D>C | D. | 离子半径:D>C>B>A |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
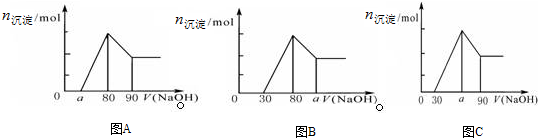
| A. | a的取值范围为 0≤a<50 | |
| B. | $\frac{n(Mg)}{n(Al)}$的最大值为2.5 | |
| C. | 若将关系图改为B图时,则a的取值范围为80<a<90 | |
| D. | 若将关系图改为C图时,则a的取值范围为75<a<90 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯属于不饱和烃,乙烷属于饱和烃 | |
| B. | 乙烯分子中所有原子处于同一平面上,乙烷分子则为立体结构,原子不在同一平面上 | |
| C. | 乙烯和乙烷燃烧现象相同,完全燃烧产物也相同 | |
| D. | 乙烯能使酸性高锰酸钾溶液褪色,乙烷不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
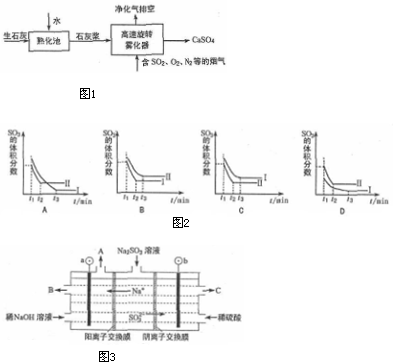
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Be2+离子中的质子和电子 | B. | H原子中的中子和质子 | ||
| C. | NaHCO3晶体中的阳离子和阴离子 | D. | Na2O2固体中的阴离子和阳离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com