
���� ��1��KClO3��H2SO4��������SO2��Ӧ�Ƶö������ȣ�ͬʱ��������أ��Դ���д��
��2��Na2CO3•3H2O2����Na2CO3��H2O2��˫�����ʣ���̼����ֻ�����˻�ԭ��Ӧ����ѡ���е����ʾ��л�ԭ�ԣ�
��3��HClO2��ClO2��+H++Cl-+H2O�У�ClԪ����+3����Ϊ+4����+3����Ϊ-1�ۣ��÷�ӦΪ5HClO2��4ClO2��+H++Cl-+2H2O��
��4�����������£���������Ӿ���ǿ�����ԣ���������NO3-��Fe3+����ԭ��Fe2+��NH4+�����Ը÷�Ӧ����������NO3-����ԭ����Fe2+����Ӧ���л�����H+������Ԫ���غ�֪���������л�����H2O��������ӦΪ8Fe2++NO3-+10H+=8Fe3++NH4++H2O���������
��� �⣺��1��KClO3��H2SO4��������SO2��Ӧ�Ƶö������ȣ�ͬʱ��������أ������ӷ�ӦΪ2ClO3-+SO2=2ClO2+SO42-��
�ʴ�Ϊ��2ClO3-+SO2=2ClO2+SO42-��
��2��Na2CO3•3H2O2����Na2CO3��H2O2��˫�����ʣ���̼����ֻ�����˻�ԭ��Ӧ����ѡ���е����ʾ��л�ԭ�ԣ�ֻ��Dѡ����ϣ��ʴ�Ϊ��D��
��3��HClO2��ClO2��+H++Cl-+H2O�У�ClԪ����+3����Ϊ+4����+3����Ϊ-1�ۣ��÷�ӦΪ5HClO2=4ClO2��+H++Cl-+2H2O����5mol�����ʷֽ�ת��4mol���ӣ�����1molHClO2�����ֽⷴӦʱ��ת�Ƶĵ�������0.8NA��4.816��1023�����ʴ�Ϊ��0.8NA��4.816��1023����
��4�����������£���������Ӿ���ǿ�����ԣ���������NO3-��Fe3+����ԭ��Fe2+��NH4+�����Ը÷�Ӧ����������NO3-����ԭ����Fe2+����Ӧ���л�����H+������Ԫ���غ�֪���������л�����H2O��������ӦΪ8Fe2++NO3-+10H+=8Fe3++NH4++H2O���÷�Ӧ��NԪ�ػ��ϼ���+5��Ϊ-3�ۡ�FeԪ�ػ��ϼ���+2�۱�Ϊ+3�ۣ�������������NO3-����ԭ����Fe2+����ԭ���������������ʵ���֮��Ϊ8��1���ʴ�Ϊ��8��1��
���� ���⿼���ȼ��仯��������ʣ�Ϊ��Ƶ���㣬����������ԭ��Ӧ�Ŀ��飬ע��������ԭ��Ӧ��Ԫ�صĻ��ϼ۱仯������ת�Ƶļ����ǽ��Ĺؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaClO | B�� | NaCl | C�� | NaOH | D�� | Na2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͨ��CH4�ĵ缫Ϊ���� | |
| B�� | �ŵ�ʱ��Һ�е����������ƶ� | |
| C�� | �����ĵ缫��ӦʽΪ��CH4+10OH--8e-�TCO32-+7H2O | |
| D�� | ͨ��CH4�ĵ缫��ӦʽΪ��CH4+2O2+4e-�TCO2+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
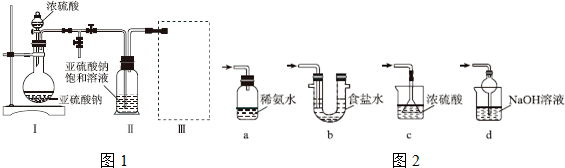

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ӧ���е��������ʻ�Ϊͬ�������� | |
| B�� | ��Ӧ����HCNO�������� | |
| C�� | ��Ӧ����N2��������������ǻ�ԭ���� | |
| D�� | ��Ӧ����NO2�ǻ�ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
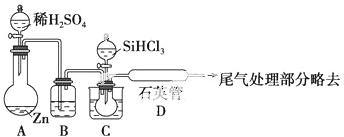
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3 | B�� | 4 | C�� | 5 | D�� | 6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ñ���NaHCO3��Һ��CO2�е��Ȼ������� | |
| B�� | SO2����ϩ�Ļ����������ͨ�����Ը��������Һ��Ũ����ϴ����ɵõ�������SO2 | |
| C�� | �þƾ���ȡ��ˮ�еĵⵥ�� | |
| D�� | ��CaO����Cl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com