

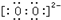 ;
;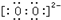 ,故答案安为:
,故答案安为: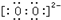 ;
;

科目:高中化学 来源: 题型:
| 序号 | 第一组 | 第二组 | 第三组 | 第四组 |
| t/℃ | 30 | 40 | 50 | 80 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 | 2.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
7 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 科学家发现的钇钡铜氧化合物在90K具有超导性,若该化合物晶体的晶胞结构如图所示,则该化合物的化学式可能是( )
科学家发现的钇钡铜氧化合物在90K具有超导性,若该化合物晶体的晶胞结构如图所示,则该化合物的化学式可能是( )| A、YBa2Cu3O3.25 |
| B、YBa2Cu3O5 |
| C、YBa2Cu2O5 |
| D、YBaCu2O3.25 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、③④ | D、①④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com