
| A. | 将少量SO2气体通入NaClO溶液中:SO2+H2O+2ClO-=SO32-+2HClO | |
| B. | 将2molSO3气体通入一密闭容器中,达平衡后吸收QkJ热量,则该反应的热化学方程式为:2SO3(g)?2SO2(g)+O2(g)△H=+Q kJ/mol | |
| C. | 向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应:4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2 | |
| D. | 用惰性电极电解MgCI2溶液:2 Cl-+2H2O=CI2↑+H2↑+2OH- |
分析 A.次氯酸根离子能够氧化二氧化硫生成硫酸根离子;
B.可逆反应不能进行到底;
C.二价铁离子还原性强于溴离子;
D.氢氧化镁为沉淀应保留化学式.
解答 解:A.少量二氧化硫通入次氯酸钠溶液中:SO2+3ClO-+H2O=SO42-+2HClO+Cl-,故A错误;
B.将2molSO3气体通入一密闭容器中,达平衡后吸收QkJ热量,2SO3(g)?2SO2(g)+O2(g)△H>+Q kJ/mol,故B错误;
C.向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应,离子方程式:4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2,故C正确;
D.用惰性电极电解MgCI2溶液:Mg2++2 Cl-+2H2O=CI2↑+H2↑+Mg(OH)2↓,故D错误;
故选:C.
点评 本题考查了离子方程式的书写,熟悉反应的实质是解题关键,注意化学式的拆分、反应物用量对化学反应的影响,题目难度中等.


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:解答题
 某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积,请回答以下问题.该小组设计的简易实验装置如图所示:
某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积,请回答以下问题.该小组设计的简易实验装置如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制银氨溶液:向稀的AgNO3溶液中逐滴加入稀氨水至刚好生成沉淀 | |
| B. | 除去苯中的少量苯酚:加入浓溴水然后过滤 | |
| C. | 除去乙酸乙酯中的少量乙酸:加入饱和碳酸钠溶液,充分振荡,静置分液,弃水层 | |
| D. | 检验溴乙烷中的溴:将溴乙烷与NaOH溶液共热后冷却,再滴加AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池工作时,锌失去电子 | |
| B. | 电池工作时,电子由正极通过外电路流向负极 | |
| C. | 电池正极的电极反应式为:2MnO2+H2O+2e-═Mn2O3+2OH- | |
| D. | 外电路中每通过0.2 mol电子,锌的质量理论上减小6.5 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 准确称取0.4000g的NaOH固体配成1000mL浓度为0.01000 mol•L-1的溶液 | |
| B. | 用硫粉覆盖地下撒有的汞;用热碱溶液洗去试管内壁的硫;用二氧化碳扑灭金属钠引起的失火;用湿润的红色石蕊试纸检验氨气是否集满;以上操作均合理 | |
| C. | 用激光笔鉴别Fe(OH)3胶体和Fe(SCN)3溶液 | |
| D. | SO2溶于水,其水溶液能导电,说明SO2是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,
,
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
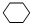 ,名称是环己烷.
,名称是环己烷.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com