
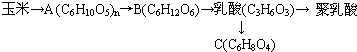
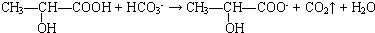
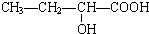 ��
��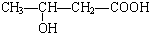 ��
��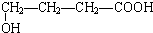
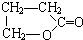 ��
�� ���� ��1��������һ�ֺ���ȡ���������ᣬ�ṹ��ʽΪCH3CHOHCOOH���������C��Ϊ���������ᷴӦ����C��ˮ��
��2�����Ậ-OH��-COOH������ˮ�γ������
��3�����Ậ-COOH����̼�����Ʒ�Ӧ��
��4����A��B���ƾ������Ҵ���һ������������Aˮ�����������ǣ������Ƿ����ƻ���Ӧ�����Ҵ��Ͷ�����̼��
��5������ʽΪC4H8O3���������������ͬ�����ţ���-OH��-COOH����̼��Ϊֱ�������ƶ������ŵ�λ�ü��ɣ���Ũ�����������ܹ����ɺ���Ԫ�����л���D��ֻ��-OH��-COOH�ڶ�Cԭ���Ϸ��ϣ�
��� �⣺��1��������һ�ֺ���ȡ���������ᣬ�ṹ��ʽΪCH3CHOHCOOH��������Ϊ�Ȼ����ǻ����������C��Ϊ���������ᷴӦ����C��ˮ��Ϊ������Ӧ����ȡ����Ӧ����
�ʴ�Ϊ���Ȼ����ǻ���������Ӧ����ȡ����Ӧ����
��2�����Ậ-OH��-COOH������ˮ�γ��������������ˮ���ʴ�Ϊ��a��
��3�����Ậ-COOH����̼�����Ʒ�Ӧ�������ӷ�ӦΪ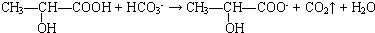 ��
��
�ʴ�Ϊ��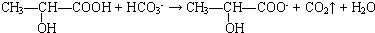 ��
��
��4����A��B���ƾ������Ҵ���һ������������Aˮ�����������ǣ������Ƿ����ƻ���Ӧ�����Ҵ��Ͷ�����̼����Ӧ�ֱ�Ϊ��C6H10O5��n+nH2O$\stackrel{����}{��}$nC6H12O6��C6H12O6$\stackrel{����}{��}$2C2H5OH+2CO2����
�ʴ�Ϊ����C6H10O5��n+nH2O$\stackrel{����}{��}$nC6H12O6��C6H12O6$\stackrel{����}{��}$2C2H5OH+2CO2����
��5������ʽΪC4H8O3���������������ͬ�����ţ���-OH��-COOH����̼��Ϊֱ�������ƶ������ŵ�λ�ü��ɣ�������������л���Ľṹ��ʽΪ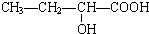 ��
��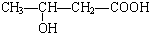 ��
��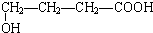 ��ֻ��
��ֻ��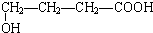 ����Ũ�����������ܹ����ɺ���Ԫ�����л���D��D�Ľṹ��ʽΪ
����Ũ�����������ܹ����ɺ���Ԫ�����л���D��D�Ľṹ��ʽΪ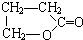 ��
��
�ʴ�Ϊ��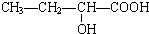 ��
��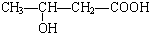 ��
��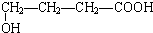 ��
��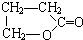 ��
��
���� ���⿼���л�����Ʊ�ʵ�飬Ϊ��Ƶ���㣬�����л���Ľṹ�����ʡ��л���ӦΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��ͬ���칹����ƶϣ���Ŀ�ѶȲ���


 ���ݼ���ϵ�д�
���ݼ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
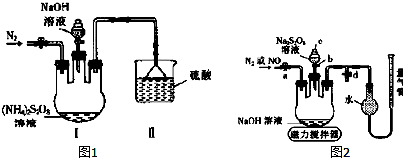
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
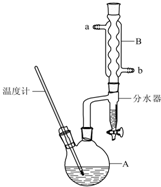 �����ѳ������л���Ӧ���ܼ���ʵ�����Ʊ������ѵķ�Ӧ����Ҫʵ��װ�����£�
�����ѳ������л���Ӧ���ܼ���ʵ�����Ʊ������ѵķ�Ӧ����Ҫʵ��װ�����£�| ��Է������� | �е�/�� | �ܶ�/g•cm3 | ˮ���ܽ��� | |
| ������ | 74 | 117.2 | 0.8109 | �� |
| ������ | 130 | 142.0 | 0.7704 | �������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 2SO2��g��+O2��g��?2SO3��g����H=-198kJ•mol-1��Ӧ���̵������仯��ͼ��ʾ����ش��������⣺
2SO2��g��+O2��g��?2SO3��g����H=-198kJ•mol-1��Ӧ���̵������仯��ͼ��ʾ����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
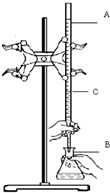 ��ʵ��������֪Ũ�ȵ�����ζ�ijδ֪Ũ�ȵ�NaOH��Һ��װ�úͲ�������ͼ��ʾ����ش�
��ʵ��������֪Ũ�ȵ�����ζ�ijδ֪Ũ�ȵ�NaOH��Һ��װ�úͲ�������ͼ��ʾ����ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
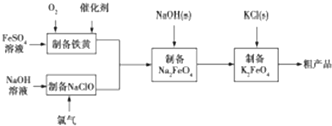
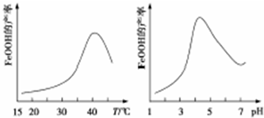
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | A | B | C | D |
| ���� | Ũ���� | �ƾ� | ���� | ����� |
| ��ǩ |  |  |  |  |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | BaSO4������ˮ������BaSO4�Ƿǵ���� | |
| B�� | ������ʵĵ�����һ����ǿ������� | |
| C�� | 25��ʱ0.1mol/L��CH3COOH��ҺpH=3��˵��CH3COOHΪ������� | |
| D�� | ij�����ܵ��磬���Ը�����һ���ǵ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com