
| 10g |
| 40g/mol |
| 1000ρω |
| M |
| 10g |
| 40g/mol |
| 10g |
| 10g+45g |
| 10 |
| 55 |
1000×1×
| ||
| 40 |


 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案科目:高中化学 来源: 题型:
| A、水是一种非常稳定的化合物,这是由于氢键所致 |
| B、乙醇分子中有一个手性碳原子 |
| C、离子晶体的晶格能越大离子键越强 |
| D、电负性Na>Al |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
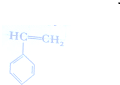 )是一种重要的化工原料,可制备聚苯乙烯塑料
)是一种重要的化工原料,可制备聚苯乙烯塑料查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁与Cl2、盐酸均能发生反应,但生成的含铁物质组成不同 |
| B、分别加热蒸干并灼烧铁、铝的氯化物溶液,最后得到的物质均为金属氧化物 |
| C、常温下,铁片、铝片与浓硫酸的反应均只能停留在金属的表面上 |
| D、等物质的量的Na、Cu、Al与足量氯气反应时,消耗的氯气一样多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、a=b | ||
| B、混合液中,c(B+)=c(A-)+c(OH-) | ||
| C、混合液的pH=7 | ||
D、混合液中,c(H+)=
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com