
实验室从含溴化氢的废液中提取溴单质,下列说法中能达到实验目的的是( )

A.用装置甲氧化废液中的溴化氢 B.用装置乙分离CCl4层和水层
C.用装置丙分离CCl4和液溴 D.用仪器丁长期贮存液溴
科目:高中化学 来源:2016-2017学年四川省高一11月月考化学卷(解析版) 题型:选择题
NA表示阿伏加德罗常数的值,下列叙述正确的是
A.将足量Na、Mg、A1分别投入到含0.5 mol的HCl的溶液中,转移电子数均为0.5 NA
B. 将lmolCO2、H2O蒸气混和物通过足量Na2O2,气体分子数变为0.5 NA
C.将含有1mol Na2CO3的溶液逐滴加入到含1.5molHCl的溶液中,产生气体分了数目为0.5NA个
D. 1molNa2O2与足量CO2反应转移的电子数为2NA个
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三上学期第三次质检化学试卷(解析版) 题型:实验题
新切开的苹果在空气中放置一段时间表面会变黄,最终变成褐色,这种现象在食品科学上通常称为“褐变”。 关于苹果褐变的原因有以下两种说法:为____________
A.苹果中的Fe2+被空气中的氧气氧化成了Fe3+
B.苹果中的酚类物质被空气中的氧气氧化了
究竟哪种说法正确,某小组同学通过实验进行了探究。
实验用品:苹果、浓度均为0.1mol·L-1的盐酸、NaHCO3溶液、Na2SO3溶液,KSCN溶液,去氧蒸馏水。
(1)探究1:
实验操作 | 实验现象 | 结论 |
在“褐变”后的苹果上滴上2~3滴 溶液。 | _________________ | 说法A不正确 |
(2)探究2:【查阅文献】Ⅰ.苹果中含有多种酚和酚氧化酶,苹果中酚氧化酶的活性温度为35℃左右、活性pH约为5.5-7.5。Ⅱ.酚类物质遇FeCl3溶液常发生显色反应而呈现一定颜色,如苯酚显紫色,对苯二酚显绿色,甲基苯酚显蓝色。
该小组将刚削皮的苹果切成七块,分别进行如下实验。请填写下表中相应的结论:
序号 | 实验步骤 | 现 象 |
|
① | 在一块上滴加2至3滴FeCl3溶液 | 表面变为绿色 | ______________ |
② | 再取两块,一块放置于空气中,另一块迅速浸入经过去氧的蒸馏水中。 | 前者表面逐渐褐变,后者相当长一段时间内,无明显变化。 | 苹果褐变与_________有关 |
③ | 另两块分别立刻放入沸水和0.1mol·L–1盐酸中浸 | 相当长一段时间内,两块均无明显变化。 | 苹果褐变与酚氧化酶的活性有关 |
④ | 最后两块分别立刻放入浓度均为0.1mol·L–1的NaHCO3和Na2SO3溶液里浸泡2min后取出,置于空气中。 | 前者经过一段时间表面逐渐褐变,后者相当长一段时间内,无明显变化。 | 亚硫酸钠溶液能阻止苹果褐变 |
(3)问题分析:Ⅰ、常温下,浓度均为0.1 mol· L-1 NaHC O3溶液略显碱性,而NaHSO3溶液却略显酸性。 NaHSO3溶液略显酸性是因为 。
O3溶液略显碱性,而NaHSO3溶液却略显酸性。 NaHSO3溶液略显酸性是因为 。
Ⅱ、0.1mol· L–1的NaHCO3溶液和Na2SO3溶液的pH相近,Na2SO3溶液却能阻止苹果褐变,结合离子方程式分析原因 : 。
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三上学期第三次质检化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的值。下列说法正确的是
A.室温下,1L pH=1的盐酸中,由水电离的H+离子数目为0.1NA
B.标况下,11.2L NO2 所含的分子数目为0.5 NA
C.甲烷碱性燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为4NA
D.1 mol C2H6O分子中含有的O—H键数目一定为NA
查看答案和解析>>
科目:高中化学 来源:2017届山东省日照市高三上学期期中化学试卷(解析版) 题型:推断题
W、X、Y、Z是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊、庚是由其中的两种、三种或四种元素组成的化合物,己是由Y元素形成的单质,常温下丙和己均为气体,丁为强碱。已知反应:①甲+乙→丁+己,②庚→乙+丙+戊。
完成下列问题:
(1)元素X在周期表中的位置为______________。
(2)元素Y、Z的简单离子的半径大小顺序为r(___________)>r(__________)。(填化学符号)
(3)化合物甲中的阴阳离子的个数比为______________。
(4)质量为a g的甲与足量的乙完全反应转移的电子数为__________。(用NA表示阿伏加德罗常数的值)
(5)写出反应“丁+庚→乙+戊”的离子方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源:2017届山东省日照市高三上学期期中化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.6.0 g SiO2晶体中含有的分子数为0.1NA
B.3.2g S2和S4的混合物中所含硫原子数一定为0.2NA
C.标准状况下,22.4 L NO和11.2 L O2混合后气体的分子总数小于NA
D.在反应KClO3+6HCl=KCl+3C12↑+3H2O中,当得到标准状况下67.2 L Cl2时,反应中转移的电子数为6NA
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期第三次月考化学试卷(解析版) 题型:实验题
甲、乙两同学欲分别完成“钠与氯气反应”的实验。
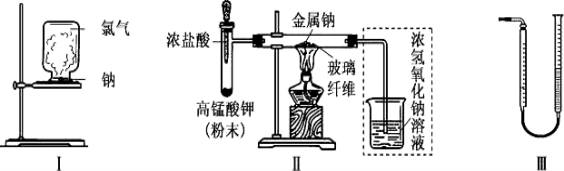
I.甲同学的方案为:取一块绿豆大的金属钠(除去氧化层),用滤纸吸净煤油,放在石棉网上,用酒精灯微热。待钠熔成球状时,将盛有氯气的集气瓶抽去玻璃片后倒扣在钠的上方(装置如图工)。该方案的不足之处有 。
Ⅱ.乙同学所采用的装置如图Ⅱ,回答下列问题:
(1)按图Ⅱ组装仪器、添加药品,实验开始后,先将浓盐酸挤入试管,试管中发生反应的离子方程式为 ;待整套装置中 后,点燃酒精灯。
(2)点燃酒精灯后,玻璃管中出现的现象是__________________。
(3)乙同学欲将虚框内装置改为图III,所示装置,并测量多余气体的体积。
①为提高测量的准确性,图III,量气管装置中的液体可用 ;收集完气体后并读数,读数前应进行的操作是冷却至室温并 。
②若未冷却至室温立即按上述操作读数,则会导致所观测气体的体积 (填“偏大”“偏小”或“无影响”,下同)。
③如果开始读数时操作正确,最后读数时俯视右边量气管液面,会导致所测气体的体积 。
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上第三次周考化学卷(解析版) 题型:选择题
某兴趣小组探究SO2气体还原Fe3+,他们使用的药品和装置如下图所示,下列说法不合理的是
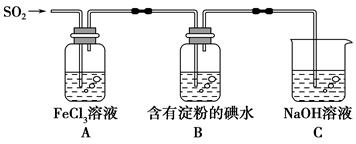
A.能表明I-的还原性弱于SO2的现象是B中蓝色溶液退色
B.装置C的作用是吸收SO2尾气,防止污染空气
C.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的BaCl2溶液,产生白色沉淀
D.为了验证A中发生了氧化还原反应,加入KMnO4溶液,紫红色退去
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:选择题
下列实验过程始终无明显现象的是
A. CO2气体通入Ba(NO3)2溶液中 B. NO2气体通入FeSO4溶液中
C. H2S气体通入CuSO4溶液中 D. HCl气体通入NaSiO3溶液中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com