
| A、它们都不是电解质 |
| B、在常温下它们都是无色气体 |
| C、它们都能与NaOH溶液发生反应 |
| D、所含碳、硫元素都是+4价,它们都有还原性 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、14.3% | B、12.5% |
| C、87.5% | D、无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 短周期主族元素A、B、C、D、E,原子序数依次增大,A元素的单质常温常压下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物甲与其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的.
短周期主族元素A、B、C、D、E,原子序数依次增大,A元素的单质常温常压下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物甲与其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、植物油不能使溴的四氯化碳溶液褪色 |
| B、葡萄糖能发生氧化反应和水解反应 |
| C、淀粉水解的最终产物是葡萄糖 |
| D、蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用茚三酮溶液可以鉴别甘氨酸与醋酸 |
| B、中和滴定实验中,用于盛放待测液的锥形瓶洗净后未干燥不会影响测定结果 |
| C、现代仪器分析中,常用质谱仪、元素分析仪、红外光谱仪等测定有机物结构,用原子吸收光谱确定物质中含有哪些非金属元素 |
| D、如果不慎将苯酚沾到皮肤上,应立即用酒精洗涤,再用水冲洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:
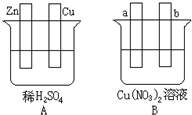 按要求对如图中两极进行必要的联接并填空,a、b为惰性材料.
按要求对如图中两极进行必要的联接并填空,a、b为惰性材料.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 |
| B、若单位时间内生成x mol N2的同时,消耗2x molNH3,则反应达到平衡状态 |
| C、达到化学平衡时,2v正(H2)=3v逆(NH3) |
| D、加入催化剂,正反应速率增大,逆反应速率不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com