
某元素只存在两种天然同位素,且在自然界它们的含量相近,其相对原子质量为152.0,原子核外的电子数为63。下列叙述中错误的是( )
A.它是副族元素
B.它是第6周期元素
C.它的原子核内有63个质子
D.它的一种同位素的核内有89个中子
科目:高中化学 来源: 题型:
常见的五种盐A、B、C、D、E,它们的阳离子可能是Na+、NH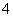 、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO
、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO 、SO
、SO 、CO
、CO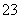 ,已知:
,已知:
①五种盐均溶于水,水溶液均为无色。
②D的焰色反应呈黄色。
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失。
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀。
请回答下列问题:
(1)五种盐中,一定没有的阳离子是____________;所含阴离子相同的两种盐的化学式是__________________。
(2)D的化学式为__________________,D溶液显碱性的原因是________________________(用离子方程式表示)。
(3)A和C的溶液反应的离子方程式是_______________________________;
E和氨水反应的离子方程式是____________________________________________。
(4)若要检验B中所含的阳离子,正确的实验方法是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某高分子材料的结构如图所示:
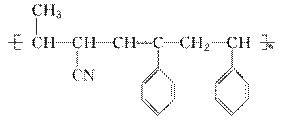
已知该高分子材料是由三种单体聚合而成的,以下与此高分子材料相关的说法正确的是 ( )。
A.该高分子材料是体型高分子,合成它的反应是加聚反应
B.形成该高分子材料的单体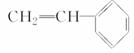 中,所有原子可能处于同一平面内
中,所有原子可能处于同一平面内
C.三种单体中有两种有机物互为同系物
D.三种单体都可以使溴水褪色,但只有两种能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于微粒半径的叙述中,正确的是( )
A.金属阳离子的半径大于它的原子半径
B.金属阳离子的半径小于它的原子半径
C.非金属阴离子的半径与其原子半径相等
D.非金属阴离子的半径小于其原子半径
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D为原子序数小于18的四种元素:
①A原子的电子层数等于最外层电子数;
②A与B处于同一周期,B与D可形成离子化合物D2B,该化合物的水溶液显碱性;
③C的离子核内质子数与核外电子数之和为18;
④A、C、D三种元素的离子具有相同的电子层排布。推断A~D各为何种元素,并填空:
(1)A________;B________;C________;D________。
(2)各原子形成简单离子的电子排布式。
(3)四种元素离子半径的大小顺序为______________________________。
(4)用离子方程式表示D2B水溶液呈碱性的原因:___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
Cu+基态核外电子排布式为
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com