
| A. | 苯萃取碘水中的I2,分出水层的操作为从上口倒出 | |
| B. | 在未知溶液中滴加BaCl2溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知溶液中存在SO42-或SO32- | |
| C. | 做蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防暴沸.如果在沸腾前发现忘记加沸石,应立即停止加热,冷却后补加 | |
| D. | 配制245mL0.1 mol•L-1的NaOH溶液,需要245mL容量瓶 |
分析 A.苯的密度比水的密度小,则萃取后下层为水;
B.白色沉淀可能为AgCl;
C.蒸馏时,防止暴沸,温度高时加沸石时液体飞溅;
D.容量瓶具有固定的规格.
解答 解:A.苯的密度比水的密度小,则萃取后下层为水,则从分液漏斗的下口放出水层,故A错误;
B.白色沉淀可能为AgCl,则原溶液中可能含银离子,故B错误;
C.蒸馏时,防止暴沸,温度高时加沸石时液体飞溅,则立即停止加热,冷却后补加,故C正确;
D.容量瓶具有固定的规格,则选择500mL容量瓶配制245mL0.1 mol•L-1的NaOH溶液,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握混合物分离提纯、离子检验、溶液的配制、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:多选题
| A. | 对于反应:H2(g)+Cl2(g)=2HCl (g)△H=-a kJ/mol,表明破坏旧化学键吸收的能量比形成新化学键释放的能量多 | |
| B. | 2MnO(s)+O2(g)═2MnO2(s),该反应在低温下能自发进行,则其△H<0 | |
| C. | 用干燥的pH试纸测得某氯水的pH=3.1 | |
| D. | 航行在大海中的轮船水面上的部分比水面下的部分腐蚀得慢,因为水下易发生电化学腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小苏打可以与胃酸反应,可用小苏打治疗胃酸过多 | |
| B. | 用浸泡过高锰酸钾溶液的硅藻土保鲜水果发生了加成反应 | |
| C. | 食品脱氧剂(含铁粉、氯化钠、炭粉等)的脱氧原理与钢铁的吸氧腐蚀相同 | |
| D. | 加人足量氢氧化钠溶液共热.能区别地沟油(加工过的餐饮废弃油)与矿物油(汽油、煤油、柴油等) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10 mL 0.5 mol/L CH3COONa溶液与6 mL 1 mol/L盐酸混合:c(Cl-)>c(Na+ )>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | 0.1 mol/L pH为3的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) | |
| C. | 硫酸氢铵溶液中滴加氢氧化钠至溶液恰好呈中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH- )=c(H+) | |
| D. | c(NH4+ )相等的(NH4)2SO4溶液、(NH4)2Fe (SO4)2溶液和NH4Cl溶液:c[(NH4)2SO4]<c[(NH4)2Fe (SO4)2]<c(NH4Cl) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{4c-b-2a}{2}$ kJ | B. | $\frac{4c+b-2a}{2}$ kJ | C. | (4c+b-2a) kJ | D. | (4c-b+2a) kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
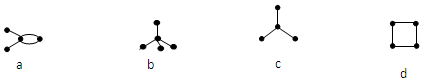
| A. | a和d是同分异构体 | B. | b和c是同系物 | ||
| C. | a和d都能发生加成反应 | D. | 只有a能使使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
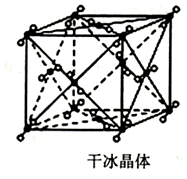 尿素(H2NCONH2)是一种农业生产中常用的氮肥.在工业上,尿素还用于制造有机铁肥,回答下列问题:
尿素(H2NCONH2)是一种农业生产中常用的氮肥.在工业上,尿素还用于制造有机铁肥,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com