
| A. | Cl-、Mg2+、AlO2-、Zn2+、SO42- | B. | Na+、Ba2+、NO3-、OH-、SO42- | ||
| C. | K+、NO3-、SO42-、OH-、Na+ | D. | MnO4-、K+、Cl-、H+、SO42- |
分析 NH4HCO3可与碱反应生成氨气,与酸反应生成二氧化碳气体,溶液与NH4HCO3作用能产生气体,此溶液可能呈酸性,也可能呈碱性,如离子之间不发生任何反应,则可大量共存,注意题目无色要求,以此解答该题.
解答 解:溶液与NH4HCO3作用能产生气体,溶液可能呈酸性,也可能呈碱性,
A.Mg2+、AlO2-可发生互促水解反应,且碱性条件下Mg2+不能大量共存,酸性条件下AlO2-不能大量共存,故A错误;
B.Ba2+、SO42-反应生成沉淀,不能大量共存,故B错误;
C.碱性条件下,离子之间不发生任何反应,可大量共存,故C正确;
D.MnO4-有颜色,不符合题目无色要求,故D错误.
故选C.
点评 本题考查离子共存的正误判断,为中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,正确理解题干条件为解答本题的关键.


科目:高中化学 来源: 题型:选择题

| A. | 该硫酸的物质的量浓度为1.84mol/L | |
| B. | 稀释该硫酸时,应将蒸馏水沿玻璃棒缓慢注入其中 | |
| C. | 配制200mL4.6mol•L-1的稀硫酸需取该硫酸50.0mL | |
| D. | 常温下,5.6gFe与足量的稀硫酸反应转移电子的物质的量为0.3mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 室温下,向1L 0.10mol•L-1 CH3COOH溶液中通人HCl至溶液pH=7时溶液中氯离子与醋酸根离子的微粒数目之和为0.2NA | |
| B. | 25℃时,1L pH=12的NaOH溶液中,由水电离的H+数目为0.01NA | |
| C. | 氢氧燃料电池负极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | H2SO4(浓)+H2S=SO2↑+S↓+2H2O反应中,生成64gSO2时,转移的电子数目为6NA. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 日常生中无水乙醇常用于杀菌消毒 | |
| B. | 目前加碘盐中主要添加的是KI | |
| C. | 绿色食品是不含任何化学物质的食品 | |
| D. | “光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化物有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷分子的球棍模型: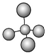 | B. | NH4Br的电子式: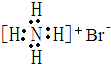 | ||
| C. | 34S2-的结构示意图: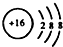 | D. | 邻羟基甲苯酸的结构简式: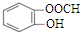 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同条件下,SO2(g)和O2(g)所具有的能量大于SO3所具有的能量 | |
| B. | 将2molSO2(g)和1molO2(g)置于一密闭容器中充分反应后,放出热量为QkJ | |
| C. | 增大压强或升高温度,该平衡都向逆反应方向移动 | |
| D. | 如将一定量SO2(g)和O2(g)置于某密闭容器中充分反应后放热QkJ,则此过程中有2molSO2(g)被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 观察钠的焰色反应需透过蓝色钴玻璃 | |
| B. | 实验室中的各种碱金属单质均保存在煤油中 | |
| C. | 配制一定物质的量浓度的溶液时容量瓶中有少量水不影响实验 | |
| D. |  为提醒人们在使用浓H2SO4时要注意安全,贮存浓H2SO4的容器上贴有图标识 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com