
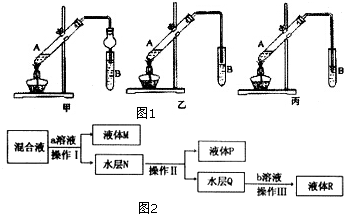
分析 (1)制取乙酸乙酯除了反应物乙醇和乙酸外,还需浓硫酸作催化剂和吸水剂,依据溶液密度大小判断加入试剂的顺序;
(2)长导管不能伸到B试管液面下,防止造成溶液倒吸入加热反应物的试管中;
(3)制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,主要是利用了乙酸乙酯难溶于饱和碳酸钠,降低乙酸乙酯溶解度,易于分层,利用萃取分液的方法分离酯,乙醇与水混溶,乙酸能被碳酸钠吸收,易于除去杂质.
解答 解:(1)制取乙酸乙酯需浓硫酸作催化剂,A试管中的液态物质有乙酸、乙醇和浓硫酸,加入试剂应先加入密度小的再加入密度大的试剂,在A试管中混合乙醇和浓硫酸的操作是:先向试管A中加入乙醇,然后缓慢的向试管注入浓硫酸,边加边振荡试管,最后加入乙酸,
故答案为:乙醇、浓硫酸、乙酸;
(2)长导管不能伸到B试管液面下,防止B试管中溶液倒吸入A试管中,丙装置B试管中导管伸入液面下,容易发生倒吸,
故答案为:丙;
(3)操作Ⅰ需要将混合液转移到分液漏斗中萃取分液,操作Ⅱ是蒸馏得到乙醇,水层为乙酸钠,加入硫酸溶液分液得到乙酸,蒸馏得到乙酸,
故答案为:分液漏斗;蒸馏;硫酸.
点评 本题考查了乙酸乙酯的制取,题目难度中等,注意掌握乙酸乙酯的制取原理及装置选择,明确反应中饱和碳酸钠溶液的作用及吸收乙酸乙酯的导管的正确处理方法.


科目:高中化学 来源: 题型:选择题
| A. | 溶液中导电粒子的数目增加,导电性增强 | |
| B. | 醋酸的电离程度增大,c(H+)减小 | |
| C. | 再加入10mL pH=11 NaOH溶液,混合液pH=7 | |
| D. | 溶液中由水电离出的c(H+)=1×10-3 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 浓度 | c(NH3)(mol/L) | c(O2)(mol/L) | c(NO)(mol/L) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.7 | 1.475 | 0.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入足量CO2后的溶液中:Na+、SiO32-、CH3COO-、SO32- | |
| B. | 饱和氯水中:Cl-、NO3-、Na+、SO32- | |
| C. | c(H+)=1×10-1 mol•L-1的溶液中:Cu2+、Al3+、SO42-、NO3- | |
| D. | 0.1 mol•L-1 CH3COONa溶液:H+、Al3+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2在Cl2中剧烈燃烧,发出黄色火焰,冒白烟 | |
| B. | SiO2的化学性质不活泼,不与任何酸发生反应 | |
| C. | 常温下,铝、铁遇浓硫酸会发生钝化反应 | |
| D. | 将氯气通入紫色石蕊试液中一些时间后,溶液变红 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com