
| A. | 一定有S2-、SO32-、Na+ | B. | 一定没有Ag+、Al3+ | ||
| C. | 可能只有Na+、S2-、CO32- | D. | 一定有Na+、S2-、NO3 |
分析 溶液中加入稀盐酸,浅黄色沉淀和气体出现,SO32-、S2-存在或者NO3-、S2-存在加入盐酸可以生成沉淀硫;出现气体可能是S2-、CO32-、SO32-离子结合氢离子生成硫化氢气体、二氧化碳气体、二氧化硫气体;溶液的焰色为黄色,则含有Na+;推断一定不含银离子,若含有银离子,则S2-、CO32-、SO32-离子都不能存在,依据离子共存判断Al3+一定不存在,所以溶液中一定含有Na+、S2-离子,S2-、CO32-、SO32-、NO3-离子可能含有.
解答 解:溶液中加入稀盐酸,浅黄色沉淀和气体出现,SO32-、S2-或者NO3-、S2-在加入盐酸后可以生成沉淀硫;出现气体可能是S2-、CO32-、SO32-离子结合氢离子生成硫化氢气体、二氧化碳气体、二氧化硫气体;溶液的焰色为黄色,则含有Na+;推断一定不含银离子,若含有银离子,则S2-、CO32-、SO32-离子都不能存在,依据离子共存判断Al3+一定不存在,所以溶液中一定含有Na+、S2-离子,S2-、CO32-、SO32-、NO3-离子可能含有;
A.此溶液中一定有Na+、S2-,而SO32-可能有,故A错误;
B.上述分析判断可知,此溶液中一定没有Ag+、Al3+,故B正确;
C.若只有Na+、S2-、CO32-,则向此溶液中加入稀盐酸,没有浅黄色沉淀出现,故C错误;
D.上述分析判断可知,此溶液中可能有SO32-或NO3-中的一种,故D错误;
故选B.
点评 本题考查了离子性质的应用和离子检验方法的分析判断,掌握离子性质的反应现象是解题关键,题目难度较大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液质量与白色固体的质量均保持不变 | |
| B. | 溶液浓度和pH值均保持不变,溶液下部是1.73g氢氧化钡固体 | |
| C. | 溶液中钡离子与氢氧根离子的数目均保持不变,${\;}^{1{8}^{\;}}$O存在于溶液和固体中,固体质量大于1.73克 | |
| D. | 溶液中钡离子与氢氧根离子的物质的量的浓度保持不变,${\;}^{1{8}^{\;}}$O存在于溶液和固体中,固体质量大于1.73克 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
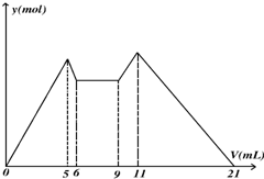
| A. | 原混合液中,c(Al3+):c(Mg2+):c(Cl-)=1:1:5 | |
| B. | A是NaOH,B是盐酸,且c(NaOH):c(HCl)=2:1 | |
| C. | 若A,B均为一元强酸或者一元强碱,则V(A):V(B)=7:13 | |
| D. | 从6到9,相应离子反应式H++OH-═H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ③④⑤ | C. | ①②⑥ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+(aq)+OH-(aq)═H2O(l)△H=+57.3kJ•mol-1 | |
| B. | 加入少量蒸馏水,平衡①和②均向右移动 | |
| C. | 溶液中c(CH3COOH)>c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| D. | 加入少量CaCl2溶液,所得溶液中:c(CH3COOH)+2c(OH-)=c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都属于氧化还原反应 | B. | 发生还原反应的元素相同 | ||
| C. | 发生氧化反应的元素不同 | D. | 生成KCl的物质的量为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com