
 2SO3 (g)��������2s����SO3��Ũ��Ϊ0.6 mol/ L���Լ��㣺(1)O2�Ļ�ѧ��Ӧ����V(O2)= �� (2)2sʱ��O2Ũ�� ��
2SO3 (g)��������2s����SO3��Ũ��Ϊ0.6 mol/ L���Լ��㣺(1)O2�Ļ�ѧ��Ӧ����V(O2)= �� (2)2sʱ��O2Ũ�� ��
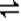 2Z 0.05mol/(l.��min) 2
2Z 0.05mol/(l.��min) 2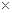 0.6/2=0 .15mol/��L��s����2sʱ��O2Ũ��=1-0 .15
0.6/2=0 .15mol/��L��s����2sʱ��O2Ũ��=1-0 .15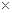 2=0.7 mol/L��
2=0.7 mol/L��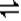 2Z�� X��ת����=0.3/1
2Z�� X��ת����=0.3/1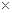 100%=30%����3����Ӧ�ӿ�ʼ��2����ĩ����Z��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊv(Z)=0.2/2/2= 0.05mol/(l.��min)����4����ͼ���Կ���������Ӧʱ��Ϊ2minʱ�������ʵ�Ũ�Ⱦ����ٱ仯�����Ե���Ӧ���е���2min���÷�Ӧ�ﵽƽ�⡣
100%=30%����3����Ӧ�ӿ�ʼ��2����ĩ����Z��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊv(Z)=0.2/2/2= 0.05mol/(l.��min)����4����ͼ���Կ���������Ӧʱ��Ϊ2minʱ�������ʵ�Ũ�Ⱦ����ٱ仯�����Ե���Ӧ���е���2min���÷�Ӧ�ﵽƽ�⡣

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
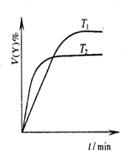
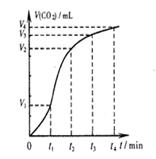
A��ͼ1��ʾ���淴Ӧ��2X��g�� Y��g����H <0�����¶�T1��T2������ Y��g����H <0�����¶�T1��T2������ |
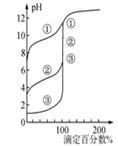
| B����0.1000 mol��L��1NaOH��Һ�ֱ�ζ�Ũ����ͬ������һԪ�ᣬ��ͼ2���߿�ȷ���ٵ�������ǿ |
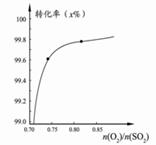
C����������������ʱ��2SO2(g) +O2(g)  2SO3(g)ת����ϵ����ͼ3���У��������ʾO2��ת���� 2SO3(g)ת����ϵ����ͼ3���У��������ʾO2��ת���� |
| D��ͼ4��ʾ̼��������ᷴӦ�ռ�����������ʱ�����t3��t4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CH3OCH3(g) +H2O(g) ��H����CO��ƽ��ת�������¶ȡ�ѹǿ�仯��ϵ��ͼ��ʾ������˵����ȷ����
CH3OCH3(g) +H2O(g) ��H����CO��ƽ��ת�������¶ȡ�ѹǿ�仯��ϵ��ͼ��ʾ������˵����ȷ����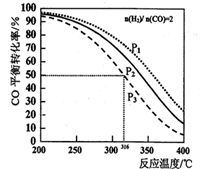
| A��������Ӧ��H>0 |
| B��ͼ��P1<P2<P3 |
| C������P3��316��ʱ�����������n(H2)=n(CH3OCH3)����ʱv(��)<v(��) |
| D������P3��316��ʱ����ʼʱn(H2)/n(CO)=3����ﵽƽ��ʱ��COת����С��50% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2NH3(g) ��H��0����һ���Ϊ2L���ܱ��ݻ��У�����0.20mol��N2��0.60mol��H2����Ӧ��NH3�����ʵ���Ũ�ȵı仯�����ͼ��ʾ��
2NH3(g) ��H��0����һ���Ϊ2L���ܱ��ݻ��У�����0.20mol��N2��0.60mol��H2����Ӧ��NH3�����ʵ���Ũ�ȵı仯�����ͼ��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
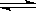 Z��g���ﵽƽ�⣬����Ӧ������ʱ��ı仯��ͼ��ʾ��������������ȷ���ǣ� ��
Z��g���ﵽƽ�⣬����Ӧ������ʱ��ı仯��ͼ��ʾ��������������ȷ���ǣ� ��
| A��X��Ũ�ȴ�С��a��b��c |
| B����������ƽ����Է�������t1ʱ��t2ʱС |
| C����c��ʱ��Ӧ�ﵽƽ�� |
| D����Ӧ�������������������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C(g)�����±�ʾ�仯ѧ��Ӧ���������ǣ� ��
2C(g)�����±�ʾ�仯ѧ��Ӧ���������ǣ� �� �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.1 mol��L��1�İ�ˮ100 mL | B��0.1 mol��L��1�Ĵ���50 mL |
| C��0.05 mol��L��1�Ĵ���100 mL | D��0.05 mol��L��1������100 mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2SO3(g) ��H<0
2SO3(g) ��H<0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NH3(g)����H��0����673 K��30 MPa�£�n(NH3)��n(H2)��ʱ��仯�Ĺ�ϵ��ͼ��ʾ��������ȷ����( )
2NH3(g)����H��0����673 K��30 MPa�£�n(NH3)��n(H2)��ʱ��仯�Ĺ�ϵ��ͼ��ʾ��������ȷ����( )
| A����a������Ӧ���ʱȵ�b�Ĵ� |
| B����c����Ӧ�ﵽƽ�� |
| C����d��t1ʱ�̣��͵�e��t2ʱ�̣���n��N2����һ�� |
| D�������������䣬773 K�·�Ӧ��t1ʱ�̣�n��H2������ͼ��d���ֵС |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com