
【题目】(1)用化学符号填空:①氯化亚铁中的阳离子 ;②标出碳酸钡中钡元素的化合价 ;③三个钙原子 .
(2)①SO3中“3”的含义: ;②Mg2+中“2”的含义: .
(3)“候氏制碱法”中的创始人
【答案】Fe2+;![]() CO3;3Ca;1个三氧化硫分子中含有三个氧原子;;1个镁离子带2个单位正电荷;;侯德榜
CO3;3Ca;1个三氧化硫分子中含有三个氧原子;;1个镁离子带2个单位正电荷;;侯德榜
【解析】(1)①氯化亚铁中的阳离子为亚铁离子表示为:Fe2+ , 故答案为:Fe2+;
②标出碳酸钡中钡元素的化合价,故可表示为:![]() CO3 , 故答案为:
CO3 , 故答案为:![]() CO3;
CO3;
③三个钙原子,就可表示为:3Ca,故答案为:3Ca;
(2)①SO3中“3”表示一个三氧化硫分子中含有3个氧原子,故答案为:1个三氧化硫分子中含有三个氧原子;
②Mg2+中“2”表示1个镁离子带2个单位的正电荷,故答案为:1个镁离子带2个单位正电荷;
(3)“候氏制碱法”中的创始人是侯德榜先生,故答案为:侯德榜.
(1)①根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字;
②元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后;
③原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字;
(2)①元素符号右下角的数字表示一个分子中的原子个数;
②元素符号右上角的数字表示每个离子所带的电荷数;
(3)“候氏制碱法”中的创始人是侯德榜先生.


 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:
【题目】“低碳循环”已引起各国家的高度重视,而如何降低大气中CO2的含量和有效地开发利用CO2正成为化学家研究的主要课题.
(1)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)
CO2(g)+H2(g),得到如下三组数据:
实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
CO | H2O | H2 | CO | |||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
3 | 900 | a | b | c | d | t |
①实验2条件下平衡常数K= .
②实验3中,若平衡时,CO的转化率大于水蒸气,则 ![]() 的值(填具体值或取值范围).
的值(填具体值或取值范围).
③实验4,若900℃时,在此容器中加入CO、H2O、CO2、H2均为1mol,则此时V正 V逆(填“<”,“>”,“=”).
(2)已知在常温常压下:写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式: .
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=﹣1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H=﹣566.0kJ/mol
③H2O(g)=H2O(l)△H=﹣44.0kJ/mol
(3)已知草酸是一种二元弱酸,草酸氢钠(NaHC2O4)溶液显酸性.常温下,向10mL 0.01molL﹣1 H2C2O4溶液中滴加10mL 0.01molL﹣1 NaOH溶液时,比较溶液中各种离子浓度的大小关系;
(4)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10﹣9 . CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10﹣4mol/L,则生成沉淀所需CaCl2溶液的最小浓度为 mol/L.
(5)以二甲醚(CH3OCH3)、空气、H2SO4为原料,铂为电极可构成燃料电池,其工作原理与甲烷燃料电池的原理相似.请写出该电池负极上的电极反应式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是:
A. 只含一种元素的物质不一定是纯净物B. 由相同元素形成的不同物质称同素异形体
C. 分子式为C2H6O的物质一定是乙醇D. C5H12只有2种同分异构体,其熔点各不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据不同的分类标准,HNO3可属于下列的哪一类
①酸 ②纯净物 ③氧化物 ④含氧酸 ⑤化合物 ⑥混合物 ⑦一元酸
A. ①②③ B. ①②④⑤⑦
C. ③④⑥ D. ①③④⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据所给的方程式写出离子方程式.
(1)Na2CO3+BaCl2═2NaCl+BaCO3↓
(2)CaCO3+2HCl═CaCl2+H2O+CO2↑
(3)CO2+2NaOH═Na2CO3+2H2O
(4)Fe2O3+6HCl═2FeCl3+3H2O
(5)Zn+2HCl═ZnCl2+H2↑ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表是元素周期表的一部分.表中所列的字母分别代表一种化学元素. 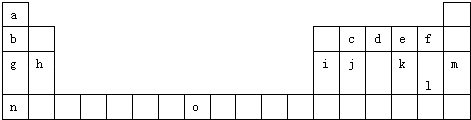
试回答下列问题:
(1)请写出字母O代表元素的外围电子排布 .
(2)由j原子跟c原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同.两者相比熔点更高的是(填化学式),试从结构角度加以解释: .
(3)白磷分子中的键角为 , 分子的空间结构为 , 每个P原子与个P原子结合成共价键.若将1分子白磷中的所有P﹣P键打开并各插入一个氧原子,共可结合个氧原子,若每个P原子上的孤对电子再与氧原子配位,就可以得到磷的另一种氧化物(填分子式).
(4)i单质晶体中原子的堆积方式如图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示. 
若已知i的原子半径为d,NA代表阿伏加德罗常数,i的相对原子质量为M,请回答:
①i单质晶体中原子的堆积方式为晶胞中i原子的配位数为 , 一个晶胞中i原子的数目为__;
②该晶体的密度为(用字母表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在酸性溶液中,下列各组离子可能共存的是( )
A.NH4+、NO3﹣、CO32﹣、Na+
B.Na+、Ba2+、NO3﹣、HCO3﹣
C.SO42﹣、Fe3+、K+、Cl﹣
D.NO3﹣、K+、SO32﹣、Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是用明矾[KAl(SO4)212H2O]制取硫酸铝和硫酸钾的操作方法,根据此图回答有关问题.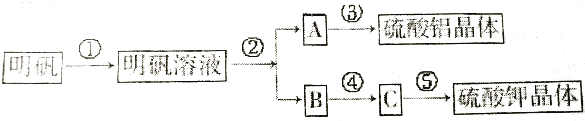
(1)进行操作②时,加入的试剂是;从反应混合物分离A所进行的实验操作是;其反应的离子方程式为;
(2)进行操作④时,所加入的试剂是 , 其目的是 , 反应混合物进行的操作是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【加试题】某研究小组按下列路线合成镇痛药哌替啶:
已知:
∣∣
请回答:
(1)A→B的反应类型是。
(2)下列说法不正确的是________。
A.化合物A的官能团是硝基
B.化合物B可发生消去反应
C.化合物E能发生加成反应
D.哌替啶的分子式是C15H21NO2
(3)写出B+C→D的化学反应方程式。
(4)设计以甲苯为原料制备C的合成路线(用流程图表示,无机试剂任选)。
(5)写出同时符合下列条件的C的所有同分异构体的结构简式。
①分子中有苯环而且是苯环的邻位二取代物;
②1H-NMR谱表明分子中有6种氢原子;IR谱显示存在碳氮双键(C=N)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com