
【题目】由下列实验及现象能推出相应结论的是( )
实验 | 现象 | 结论 | |
A | 将 | 溶液变为血红色 |
|
B | 向 | 生成白色沉淀 | 非金属性 |
C | 向盛有 | 溴水褪色 | 还原性: |
D | 向无色溶液中滴入 | 有白色沉淀生成 | 无色溶液中一定含 |
A. A B. B C. C D. D
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列叙述正确的是( )

A. 反应开始到10 s,用Z表示的反应速率为0.158 mol·L-1·s-1
B. 10 s后,该反应停止进行
C. 反应的化学方程式为2X(g)+Y(g)![]() 2Z(g)
2Z(g)
D. 0~10 s的时间内的平均反应速率:v(X)=v(Y)=0.0395 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用PbS铅精矿(主要成分为PbS,含少量杂质)碳化法炼铅是一种绿色工艺,其主要工艺流程如下:

回答下列问题:
(1)“转化”是该工艺的关键,转化时发生反应的化学方程式为2PbS+2(NH4)2CO3+O2+2H2O===2PbCO3+2S+4NH3·H2O。
①(NH4)2CO3在上述反应中________(填字母)。
a.作氧化剂b.作还原剂c.既不作氧化剂也不作还原剂
②转化时,温度对铅转化率的影响如图1所示,则适宜的转化温度范围为________。
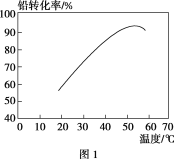
③有无FeS2对铅转化率的影响如图2所示,说明FeS2在转化中的作用是________。

(2)“溶解”时发生反应的离子方程式为________________________________。
(3)“电解”时,阴极的电极反应式为___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤族元素随着原子核电荷数的增加,下列叙述不正确的是
A.原子半径依次增大B.单质的熔沸点逐渐升高
C.卤离子的还原性逐渐减弱D.氢化物的热稳定性依次减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是一种常见的绿色氧化剂,可由臭氧发生器(原理如图)电解稀硫酸制得。下列说法错误的是
是一种常见的绿色氧化剂,可由臭氧发生器(原理如图)电解稀硫酸制得。下列说法错误的是
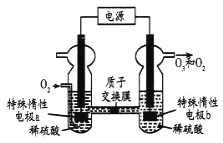
A. 电极a为阴极
B. 标准状况下,当![]() 反应时收集到
反应时收集到![]() 和
和![]() 混合气体
混合气体![]() ,
,![]() 的体积分数为80%
的体积分数为80%
C. 电解一段时间后b极周围的![]() 下降
下降
D. a极的电极反应为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室中可用下图装置来制取乙酸乙酯。回答下列问题

(1)写出制取乙酸乙酯的化学方程式__________________________;
(2)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是:_________________________________________________;
(3)浓硫酸的作用是______________;
(4)饱和碳酸钠的作用是________________________________________;
(5)通蒸气的导管要靠近饱和碳酸钠溶液的液面,但不能插入溶液之中,原因是________________________;
(6)若要将乙酸乙酯分离出来,应当采取的实验操作是___________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业碳酸钠(纯度约为98%)中含有Mg2+、Fe2+、Cl-和SO42-等杂质,提纯工艺流程如下:
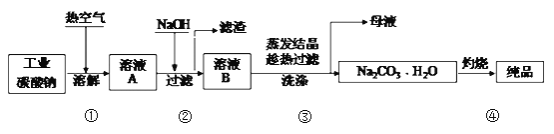
下列说法不正确的是
A. 步骤①,通入热空气可加快溶解速率
B. 步骤②,产生滤渣的离子反应为:Mg2+ + Fe3+ + 5OH- == Mg(OH)2↓+ Fe(OH)3↓
C. 步骤③,趁热过滤时温度控制不当会使Na2CO3H2O中混有Na2CO310H2O等杂质
D. 步骤④,灼烧时用到的主要仪器有铁坩埚、泥三角、三脚架、酒精灯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设计下列实验方案鉴别Na2CO3和NaHCO3两种白色粉末,不能达到预期目的的是
A. 分别向等质量的白色粉末中加等体积适量的水,比较固体溶解量的多少
B. 分别配成溶液,加入CaCl2溶液,比较是否有沉淀生成
C. 分别配成溶液,做焰色反应,观察火焰的颜色
D. 分别将等量的白色粉末用如图装置进行实验,比较澄清石灰水是否变浑浊.
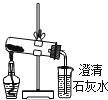
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com