
| A. | 能与金属铝反应放出氢气的溶液 | |
| B. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=10-6的溶液 | |
| C. | pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合 | |
| D. | 0.01 mol•L-1的氨水与0.01 mol•L-1的HCl溶液等体积混合 |
分析 A.铝的单质能和酸、碱都反应生成氢气;
B.常温下溶液中存在离子积c(H+)c(OH-)=10-14,$\frac{c({H}^{+})}{c(O{H}^{-})}$=10-6,代入计算分析判断氢离子浓度和氢氧根离子浓度大小;
C.pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合,pH=2的CH3COOH溶液中存在电离平衡,加入氢氧化钠溶液反应后又电离出氢离子,醋酸溶液浓度大于氢氧化钠溶液浓度,等体积混合溶液显酸性;
D.0.01 mol•L-1的氨水与0.01 mol•L-1的HCl溶液等体积混合恰好完全反应生成氯化铵溶液,溶液中铵根离子水解溶液显酸性.
解答 解:A.铝单质和稀酸反应生成铝盐和氢气,铝盐水解溶液显酸性,铝单质和强碱反应生成偏铝酸钠和氢气,偏铝酸钠溶液水解显碱性,故A错误;
B.常温下溶液中存在离子积c(H+)c(OH-)=10-14,$\frac{c({H}^{+})}{c(O{H}^{-})}$=10-6,代入计算得到,c(OH-)=10-4mol/L,c(H+)=10-10mol/L,氢离子浓度小于氢氧根离子浓度,溶液显碱性,故B正确;
C.pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合,醋酸溶液中存在电离平衡,平衡状态下氢离子浓度和pH=12的氢氧化钠溶液中氢氧根离子浓度相同,醋酸溶液浓度大于氢氧化钠溶液浓度,等体积混合反应,醋酸又电离出氢离子,溶液显酸性,故C错误;
D.0.01 mol•L-1的氨水与0.01 mol•L-1的HCl溶液等体积混合恰好完全反应生成氯化铵溶液,溶液中铵根离子水解溶液显酸性,NH4++H2O?NH3•H2O+H+,故D错误;
故选B.
点评 本题考查了物质性质、弱电解质电离平衡、盐类水解和溶液酸碱性的分析判断,注意弱电解质电离平衡的理解应用,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 亚硫酸的电离方程式:H2SO3?2H++SO${\;}_{3}^{2-}$ | |
| B. | 乙炔的分子结构模型示意图: | |
| C. | H2O2的电子式:H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$]2-H+ | |
| D. | 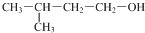 的名称3-甲基-1-丁醇 的名称3-甲基-1-丁醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
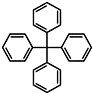
| A. | 分子式为C25H20,属于苯的同系物 | |
| B. | 该物质不能发生硝化反应 | |
| C. | 能使溴水和酸性KMnO4溶液褪色 | |
| D. | 1 mol该物质最多能与12 mol氢气发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油的催化裂化和裂解 | B. | 煤的液化、气化和煤的干馏 | ||
| C. | 漂白的草帽久置于空气中变黄 | D. | 石油的分馏和海水蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤⑥ | B. | ①④⑤ | C. | ④⑤⑦ | D. | ③⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (CH3)2CHOH | B. | (CH3)2C(C2H5)OH | C. | (CH3)3CCH2OH | D. | CH3C(C2H5)2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
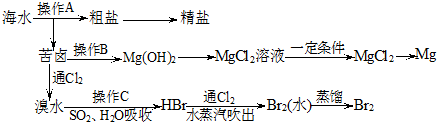
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①③④ | C. | ②④⑤ | D. | ②③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com