
为了探究木炭与浓H2SO4反应的产物中是否存在CO2,某同学选用如图所示装置进行实验:
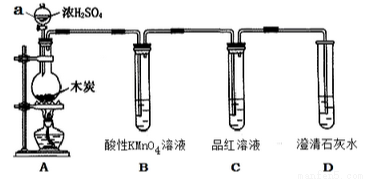
(1)仪器a的名称为:__________;在组装好上述实验装置后,在装入药品之前必需的实验操作是________________。
(2)写出A中发生反应的化学方程式____________________。该装置还可以用于实验室制取Cl2,请写出实验室制取Cl2的离子方程式并用单线桥标明电子转移________________。
(3)装置B的作用是____________________。
(4)能说明产物中一定存在CO2气体的实验现象为________________。
(5)质量分数为98%的浓硫酸,其密度为1.84g/ml,该浓硫酸的物质的量浓度为__________,用该硫酸配制500ml 0.5mol/L的稀硫酸,主要仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要____________,定容时由于俯视刻度线,则对浓度产生的影响为___________ (填“偏大”“偏小”或“无影响”)。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2017届四川省成都市高三第二次模拟考试理综化学试卷(解析版) 题型:简答题
废旧无汞碱性锌锰电池可用于制造隐形战机的机身涂料MnxZn(1-x)Fe2O4,该电池工作反应原理为Zn+2MnO2+2H2O 2MnO(OH)+Zn(OH)2。某化学小组利用废电池制涂料的工艺如下:
2MnO(OH)+Zn(OH)2。某化学小组利用废电池制涂料的工艺如下:
A.浸取:将去除表面塑料的旧电池加入水中浸取并过滤,滤液经操作a得KOH固体;
B.溶液:滤渣中加入过量稀硫酸和足量双氧水,至不再出现气泡时,过滤;
C.测成分:测步骤B中滤液成分,然后加入铁粉;
D.氧化:加入双氧水氧化;
E.调pH:滴加氨水调pH,经结晶处理得MnxZn(1-x)Fe2O4。
(1)浸取时的操作有 ______。
A.拆解、粉碎旧电池 B.降低温度 C.搅拌 D.加压
(2)操作a为________。
(3)溶渣时生成Mn2+的主要离子方程式为______________________________。
(4)若步骤C测得滤液中金属离子组成为:c(Mn2+) +c(Zn2+) =0.8mol/L, c(Fe2+ ) = 0. 1 mol/L。若滤液体积为lm3,要合成MnxZn(1-x)Fe2O4,需加入Fe粉质量为___________kg(忽略体积变化)。
(5)氧化时,因为分解所需双氧水的量比理论值大得多。其原因可能是①温度过高;②______。
(6)最后一步结晶时,处理不当易生成MnFe2O4和ZnFe2O4。要制得MnxZn(1-x)Fe2O4,最后一步结晶时需注意______________________。
(7)某小组构想用ZnSO4、MnSO4溶液为原料,以Fe作电极用电解法经过一系列步骤制得MnxZn(1-x)Fe2O4,则开始电解时阳极反应式为___________________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省滨州市高二下学期第一次阶段性测试化学试卷(解析版) 题型:填空题
元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p 轨道上有4个电子。元素Z 的原子最外层电子数是其内层的3倍。
(1)X与Y所形成化合物晶体的晶胞如右图所示。
①在1个晶胞中,X离子的数目为______。
②该化合物的化学式为__________。
(2)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是_____。
(3)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是____________________。
(4)Y 与Z 可形成YZ42-,则: YZ42-的空间构型为________________(用文字描述)。
写出一种与YZ42-互为等电子体(价电子数相同)的分子的化学式:______________。
(5)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为_________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省滨州市高二下学期第一次阶段性测试化学试卷(解析版) 题型:选择题
下列曲线表示卤族元素(F、Cl、Br)某种性质随核电荷数的变化趋势,正确的是( )
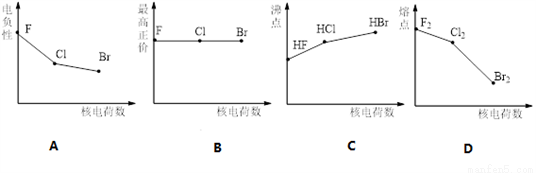
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:天津市2016-2017学年高二下学期小样提高卷化学(理)试卷(3.19) 题型:填空题
某研究性学习小组要鉴定和研究苯甲酸的结构和性质,现有苯甲酸的粗品,实验步骤如下
(1)第一步必须进行的操作名称是:_________
(2)化学组成分析
①定性分析(证明苯甲酸中含有C、H元素):取一定量的苯甲酸,在密闭容器中与氧气充分燃烧,然后将燃烧产物依次通入________和___________。
②定量分析(确定苯甲酸中C、H元素的质量分数):取一定量的苯甲酸,在密闭容器中与氧气充分燃烧, 然后将燃烧产物依次通入_______和_______。
③通过计算证明苯甲酸中是否有氧元素,并确定其质量分数。
④测定苯甲酸的相对分子质量。
(3)波谱分析法鉴定分子结构
①通过_________________可获得苯甲酸分子中含有何种化学键或官能团的信息(写方法名称)。
②从核磁共振氢谱上可判定苯甲酸分子中有________种不同类型的氢原子及它们的数目比为___________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都简阳市高一上学期期末检测化学试卷(解析版) 题型:选择题
下列实验中,依据实验操作及现象,得出的结论不正确的是 ( )
操 作 | 现 象 | 结 论 | |
A | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
B | 将一片铝箔置于酒精灯外焰上灼烧 | 铝箔熔化但不滴落 | 铝箔表面有致密Al2O3薄膜,且Al2O3熔点高于Al |
C | 无色溶液中滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
D | 向溶液X中加入稀盐酸,并将产生的无色无味气体通入澄清石灰水中 | 生成白色沉淀 | 溶液X中可能含有 CO32-或 HCO3- |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都简阳市高一上学期期末检测化学试卷(解析版) 题型:选择题
下列有关铁及其化合物的说法中正确的是
A.除去FeCl3溶液中的FeCl2杂质可以向溶液中通入氯气
B.铁与水蒸气在高温下的反应产物为Fe2O3和H2
C.Fe3O4为红棕色晶体
D.Fe(OH)2和Fe(OH)3都能在空气中稳定存在
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市高二3月学生学业能力调研化学试卷(解析版) 题型:简答题
易混易错题组
Ⅰ、官能团能体现有机物的特殊性质,认识下列有机物的官能团。
(1)C6H5CH2OH的物质类别是______
(2)非诺洛芬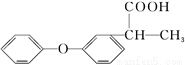 中的官能团的结构简式是__________
中的官能团的结构简式是__________
(3)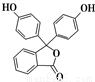 中含氧官能团的名称是______________
中含氧官能团的名称是______________
Ⅱ、按要求回答关于有机物命名的问题:
(1)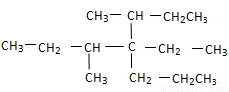
该烃主链碳原子数为_______,支链数为________,
学法题:
①烷烃选择主链的要求是____________________。
②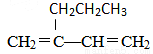 该烃的主链碳原子数为______,
该烃的主链碳原子数为______,
学法题:
(1)烯烃或二烯烃选择主链的要求是_______________。
(2)写出(CH3CH2)2C(CH3)2的系统命名___________________
(3)分子式为C6H12的某烯烃,所有的碳原子都在同一平面上,写出其结构简式:_______________,其系统命名是_____________。
查看答案和解析>>
科目:高中化学 来源:2017届浙江省绍兴市高三3月教学质量调测考试化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A. 用分液的方法可以分离汽油和水 B. 酒精灯加热试管时须垫石棉网
C. NH3能使湿润的蓝色石蕊试纸变红 D. 盛放NaOH溶液的广口瓶,可用玻璃塞
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com