
| A. | 增大压强,活化分子数增多,化学反应速率一定增大 | |
| B. | 升高温度,活化分子百分数不一定增大,化学反应速率一定增大 | |
| C. | 加入反应物,使活化分子百分数增加,化学反应速率增大 | |
| D. | 使用催化剂,降低了反应的活化能,增大了活化分子百分数,化学反应速率一定增大 |
分析 A.增大压强,使浓度增大,活化分子百分数增加;
B.升高温度,活化分子百分数增加,化学反应速率增大;
C.加入反应物,活化分子百分数不变;
D.催化剂可以降低反应的活化能,增大活化分子百分数.
解答 解:A.增大压强,使浓度增大,活化分子浓度增加,化学反应素速率增大,但活化分子数不变,故A错误;
B.升高温度,活化分子的百分数增大,反应速率增大,故B错误;
C.加入反应物,反应物的浓度增大,单位体积活化分子的数目增大,活化分子的百分数不变,故C错误;
D.催化剂可以降低反应的活化能,增大活化分子百分数,所以化学反应速率一定增大,故D正确.
故选D.
点评 本题考查活化能及其对反应速率的影响,题目难度不大,注意温度、浓度、压强、催化剂等外界条件对化学反应速率的影响的根本原因是对活化分子的影响,但影响原因不同.


科目:高中化学 来源: 题型:填空题
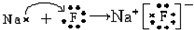 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 92.3% | B. | 87.6% | C. | 75% | D. | 84.9% |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
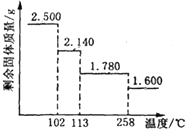 胆矾晶体(CuSO4•5H2O)中4个水分子与铜离子形成配位键,另一个水分子只以氢键与相邻微粒结合.某兴趣小组称取2.500g胆矾晶体,逐渐升温使其失水,并准确测定不同温度下剩余固体的质量,得到如图所示的实验结果示意图.以下说法正确的是 ( )
胆矾晶体(CuSO4•5H2O)中4个水分子与铜离子形成配位键,另一个水分子只以氢键与相邻微粒结合.某兴趣小组称取2.500g胆矾晶体,逐渐升温使其失水,并准确测定不同温度下剩余固体的质量,得到如图所示的实验结果示意图.以下说法正确的是 ( )| A. | 晶体从常温升至105℃的过程中只有氢键断裂 | |
| B. | 受热过程中,胆矾晶体中形成配位键的4个水分子同时失去 | |
| C. | 120℃时,剩余固体的化学式是CuSO4•H2O | |
| D. | 按胆矾晶体失水时所克服的作用力大小不同,晶体中的水分子所处化学环境可以分为3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.8×10-7mol•L-1 | B. | 1.0×10-5 mol•L-1 | ||
| C. | 1.0×10-7 mol•L-1 | D. | 1.8×10-9 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:1 | B. | 100:1 | C. | 1:100 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C60H120O60 | B. | C60H100O52 | C. | C60H102O51 | D. | C60H112O51 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com