
【题目】分析下列有机化合物,完成填空。
①CH4 ② C2H4 ③C2H2 ④![]() ⑤
⑤![]() ⑥
⑥![]() ⑦
⑦![]() ⑧
⑧![]()
(1)①~⑧中,属于苯的同系物的是____ (填序号,下同)
(2)①分子的空间构型为_____,②中碳原子的杂化方式为_____。
(3)相同质量的①②③中,在相同状况下体积最小的是___,完全燃烧时消耗O2最多的是___。
(4)以⑧为原料制备TNT的化学方程式为______。
(5)④的系统命名为:____。
(6)若将CH4、O2和氢氧化钠溶液组成燃料电池,则电池的负极反应式为___。
(7)写出⑤的含有苯环的所有同分异构体______。
【答案】⑧ 正四面体型 sp2 ② ①  3-甲基-2-戊烯 CH4-8e-+10OH-=CO32-+7H2O
3-甲基-2-戊烯 CH4-8e-+10OH-=CO32-+7H2O 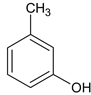 、
、 、
、 、
、
【解析】
(1)苯的同系物只含有1个苯环,且烃基为饱和烃基;
(2)①为甲烷,分子的空间构型为正四面体,②为乙烯,碳原子价层电子对数为3;
(3)相同质量的①~③中,在相同状况下体积最小,则物质的量最少,相对分子质量应最大;含氢量越大,耗氧量越多;
(4)甲苯与浓硝酸在浓硫酸作用下发生取代反应生成TNT;
(5)![]() 主链是5个碳,含碳碳双键,属于烯烃,3号碳上有甲基;
主链是5个碳,含碳碳双键,属于烯烃,3号碳上有甲基;
(6)碱性条件下,负极上甲烷失电子发生氧化反应生成碳酸根离子;
(7)从位置异构、官能团异构的角度考虑。
(1)苯的同系物只含有1个苯环,且烃基为饱和烃基,⑧符合;
(2)①为甲烷,分子的空间构型为正四面体,②为乙烯,碳原子形成1个π键、3个σ键,无孤电子对,价层电子对数为3,不含孤电子对,碳原子的杂化方式为sp2杂化;
(3)相同质量的①~③中,在相同状况下体积最小,则物质的量最少,相对分子质量应最大,应为②;含氢量越大,耗氧量越多,①符合;
(4)甲苯与浓硝酸在浓硫酸作用下发生取代反应生成TNT,反应的方程式为 ;
;
(5)![]() 主链是5个碳,含碳碳双键,属于烯烃,3号碳上有甲基,系统命名为:3-甲基-2-戊烯;
主链是5个碳,含碳碳双键,属于烯烃,3号碳上有甲基,系统命名为:3-甲基-2-戊烯;
(6)若将CH4、O2和氢氧化钠溶液组成燃料电池,碱性条件下,负极上甲烷失电子发生氧化反应生成碳酸根离子,则电池的负极反应式为CH4-8e-+10OH-=CO32-+7H2O;
(7)![]() 的含有苯环的所有同分异构体
的含有苯环的所有同分异构体 、
、 、
、 、
、 ,共4种。
,共4种。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.乙烯、聚乙烯、乙炔、聚乙炔都能使溴水或高锰酸钾溶液褪色,但与两种试剂发生反应的反应类型是不同的
B.最简单的芳香族化合物是苯,最简单的糖是葡萄糖
C.常温下苯与液溴、铁粉混合反应生成的油状有机物呈红褐色,这是溶有氢氧化铁杂质造成的
D.三氯异氰尿酸(TCCA)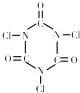 是用于游泳池等公共场合消毒的第三代产品,具有强烈的氯气刺激味,含有效氯在90%以上,结构简式如图所示.据此推测TCCA分子中氯元素显正价
是用于游泳池等公共场合消毒的第三代产品,具有强烈的氯气刺激味,含有效氯在90%以上,结构简式如图所示.据此推测TCCA分子中氯元素显正价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.字母A~K代表常见物质,在一定条件下能发生如图所示变化。
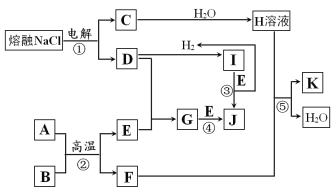
已知:反应②中A为黑色粉末,B为金属单质,且n(A):n(B)=3:2。反应③和④均在水溶液中进行。
(1)写出J的名称:___。
(2)写出反应②的化学方程式:___。
(3)写出反应⑤的离子方程式:___。
II.某研究性学习小组的同学以Fe(NO3)3溶液来探究Fe3+能否氧化Ag为题。他们选用少量的Fe(NO3)3溶液与做过银镜反应的试管进行实验。现象:银镜部分溶解,试管上方出现少量淡淡的红棕色气体。
请你判断:以上实验能否得到相关结论。
若你认为能得出结论,请简述理由:___。
若你认为不能得出结论,请在此实验基础上,再继续实验(试剂任选),直至得出相关结论。请设计实验(写出实验操作、现象和结论):___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.己烷有5种同分异构体(不考虑立体异构),它们的熔点、沸点各不相同
B.苯的密度比水小,但由苯反应制得的溴苯、硝基苯的密度都比水大
C.聚合物(![]() )可由单体CH3CH=CH2和CH2=CH2加聚制得
)可由单体CH3CH=CH2和CH2=CH2加聚制得
D.1 mol葡萄糖能水解生成2 mol CH3CH2OH和2 mol CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷能形成众多单质与化合物。回答下列问题:
(1)磷在成键时,能将一个3s电子激发进入3d能级而参加成键,写出该激发态原子的核外电子排布式__ 。
(2)黑磷是一种二维材料,其中一层的结构如图1所示。
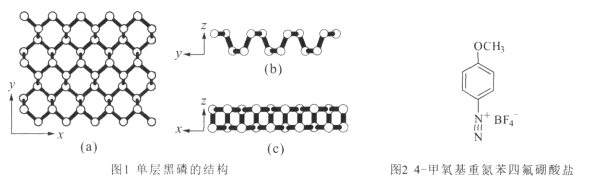
①黑磷中P原子的杂化方式为 _________ 。每一层内P形成六元环彼此相接,平均每个空间六元环中含有的磷原子是 ____个。
②用4-甲氧基重氮苯四氟硼酸盐(如图2)处理黑磷纳米材料,可以保护和控制其性质。
该盐的构成元素中C、N、O、F的电负性由大到小顺序为__,1mol该盐阳离子含有的σ键的数目为______ ,该盐阴离子的几何构型是__。
(3)磷钇矿可提取稀土元素钇(Y),某磷钇矿的结构如下:
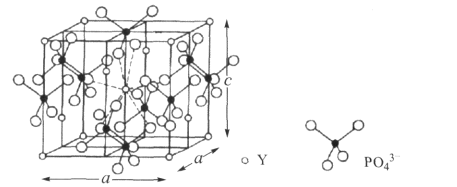
该磷钇矿的化学式为__,与PO43—互为等电子体的阴离子有__ (写出两种离子的化学式)。已知晶胞参数a= 0.69 nm,c=0.60 nm,阿伏加德罗常数为NA,则该磷钇矿的密度为__g.cm—3(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图所示装置回答以下问题。

(1)利用如图装置可以验证元素非金属性的变化规律。图中D装置的名称是__,其作用是___。
(2)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2、Na2SO3、Na2CO3、H2O2、H2SO4,请选择合适药品设计实验验证氯的非金属性强于硫:装置B中发生反应的化学方程式为:__,装置C中发生的离子方程式为:__。
(3)若要用此装置证明非金属性:S>C>Si,从以下所给物质中选择药品设计实验:①稀盐酸②稀H2SO4③CaCO3④Na2CO3⑤Na2SiO3溶液⑥SiO2。试剂B与C分别为___(填序号);装置C中发生反应的离子方程式为:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关实验室制乙烯的说法中,不正确的是 ( )
A. 温度计应伸入反应物的液面以下
B. 要向烧瓶中加入碎瓷片,以防液体受热产生暴沸
C. 乙烯气体中可能混有SO2、CO2杂质,需进一步净化处理
D. 加热要缓慢,使温度逐渐上升至170℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)按系统命名法命名:
 __________________.
__________________.
(2)按要求写出有机物的结构简式:支链只有一个乙基且相对分子质量最小的烷烃________.
(3)羟基的电子式为________.
(4)![]() 与Br2发生1,4加成反应的化学方程式为________.
与Br2发生1,4加成反应的化学方程式为________.
(5)下列说法错误的为________(填选项字母)
a.实验室制取乙烯时,将温度计的水银球插入液面以下
b.将氯乙烷溶于滴有HNO3的AgNO3溶液中,可检验氯乙烷分子中含有的氯原子
c.溴乙烷和NaOH的醇溶液混合物加热,将产生的气体直接通入酸性KMnO4溶液来检验反应是否生成了乙烯
d.将铜丝绕成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,无水乙醇可被氧化为乙醛
(6)A和B的分子式均为C2H4Br2,A的核磁共振氢谱只有一个吸收峰,则A的结构简式为___,请预测B的核磁共振氢谱有___个吸收峰。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素 X、Y、Z、W 原子序数依次增大,Y 与 W 同族。X、Y、Z 三种原子最外层电子数的关系 为 X+Z=Y。电解 Z 与 W 形成的化合物的水溶液,产生 W 元素的气体单质,此气体同冷烧碱溶液作 用,可得到化合物 ZWX 的溶液。下列说法正确的是
A.W 的氢化物稳定性强于 Y 的氢化物
B.Z与其他三种元素分别形成的化合物中只含有离子键
C.Z 与 Y 形成的化合物的水溶液呈碱性
D.对应的简单离子半径大小为 W >Z > X>Y
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com