
硫代硫酸钠(Na2S2O3·5H2O)俗名“大苏打”,又称为“海波”。在纺织工业中用于棉织品漂白后的脱氯剂、染毛织物的硫染剂、靛蓝染料的防白剂、纸浆脱氯剂、医药工业中用作洗涤剂、消毒剂和褪色剂等,它易溶于水,难溶于乙醇,加热易分解。工业上常用亚硫酸钠法、硫化碱法等制备。某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如下图:
实验具体操作步骤为:
①开启分液漏斗,使硫酸慢慢滴下,适当调节螺旋夹,使反应产生的SO2气体较均匀地通入Na2S和Na2CO3的混合溶液中,同时开启电磁搅拌器搅动。
②至析出的硫不再消失,控制溶液的pH接近7时,停止通入SO2 气体。
③抽滤所得的滤液,转移至蒸发皿中,水浴加热浓缩,直到溶液表面出现晶膜。
④冷却结晶、抽滤、洗涤。
⑤将晶体放入烘箱中,在40~450C左右干燥50~60min,称量。请回答以下问题:
(1)仪器b的名称是 ;
(2)步骤②中若控制PH值小于7,则产率会下降,请用离子方程式解释原因: 。
(3)步骤③中不能将溶液蒸发至干的原因是 ;晶膜通常在溶液表面出现的原因是 。
(4)步骤④中洗涤硫代硫酸钠晶体试剂的结构式是 。
(5)下列有关抽滤的说法中,正确的是 。
A.为了检验洗涤是否完全,应拔下吸滤瓶与安全瓶之间橡皮管,从吸滤瓶上口倒出少量洗涤液于试管中进行相关实验
B.抽滤前先用溶剂将滤纸湿润,使滤纸与漏斗底部贴紧
C.抽滤结束时应先关抽气泵,后抽掉抽滤瓶接管
D.在洗涤沉淀时,应关小水龙头,使洗涤剂缓缓通过沉淀物
(6)为检验制得的产品的纯度,该实验小组称取5.0克的产品配制成250mL硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:在锥形瓶中加入25mL 0.01mol/L KIO3溶液,并加入过量的KI并酸化,发生下列反应:5I-+IO3-+6H+=3I2+3H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应:I2+2S2O32-=2I-+S4O62-,当蓝色褪去且半分钟不变色时到达滴定终点。实验数据如下表:
| 实验序号 | 1 | 2 | 3 |
| Na2S2O3溶液体积(mL) | 19.98 | 20.02 | 21.18 |
(1)三颈烧瓶(1分)
(2)S2O32—+2H+=S↓+H2O+SO2↑(2分)
(3)蒸干会使硫代硫酸钠脱水并分解;(2分)因为溶液表面温度较低(1分)
(4)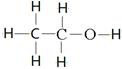 (2分)
(2分)
(5)A B D(3分)
(6) 0.93;(2分) A E(2分
解析试题分析:(1)根据仪器b的结构特点可知,其名称是三颈烧瓶。
(2)由于在酸性条件下易发生反应S2O32—+2H+=S↓+H2O+SO2↑,所以步骤②中若控制PH值小于7,产率会下降。
(3)由于硫代硫酸钠加热易分解,所以蒸干会使硫代硫酸钠脱水并分解;因为溶液表面温度较低,所以晶膜通常在溶液表面出现。
(4)硫代硫酸钠易溶于水,难溶于乙醇,所以应该用乙醇洗涤,乙醇的结构式为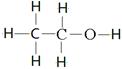 。
。
(5)A.由于在抽滤中滤液上下方形成压强差,所以为了检验洗涤是否完全,应拔下吸滤瓶与安全瓶之间橡皮管,从吸滤瓶上口倒出少量洗涤液于试管中进行相关实验,A正确;B.抽滤前先用溶剂将滤纸湿润,使滤纸与漏斗底部贴紧,B正确;C.抽滤结束时应先抽掉抽滤瓶接管,后关抽气泵,以防止倒吸,C不正确;D.洗涤晶体时,先关闭水龙头,用蒸馏水缓慢淋洗,再微接水龙头,将洗涤液慢慢透过全部晶体,D正确,答案选ABD。
(6)根据表中数据可知,第三次实验的数据误差较大,应舍去,所以消耗溶液体积的平均值为(19.98ml+20.02ml)÷2=20.00ml。根据反应式5I-+IO3-+6H+=3I2+3H2O、I2+2S2O32-=2I-+S4O62-可知IO3-~3I2~6S2O32-,所以Na2S2O3溶液浓度是 =0.075mol/L,所以250ml溶液中Na2S2O3·5H2O的质量是0.075mol/L×0.25L×248g/mol=4.65g,所以纯度为4.65g÷5.0g=0.93;A.滴定管未用Na2S2O3溶液润洗,则溶液浓度被稀释,消耗溶液的体积增加,测测定结果偏低;B.滴定终点时俯视读数,读数偏小,则消耗溶液的体积减少,测定结果偏高;C.锥形瓶用蒸馏水润洗,不影响实验结果;D.滴定管尖嘴处滴定前无气泡,滴定终点发现气泡,则消耗溶液的体积减少,则测定结果偏高;E.滴定时震荡锥形瓶较剧烈,则生成的碘离子被空气氧化生成单质碘,从而消耗溶液的体积增加,实验测定结果偏低,答案选AE。
=0.075mol/L,所以250ml溶液中Na2S2O3·5H2O的质量是0.075mol/L×0.25L×248g/mol=4.65g,所以纯度为4.65g÷5.0g=0.93;A.滴定管未用Na2S2O3溶液润洗,则溶液浓度被稀释,消耗溶液的体积增加,测测定结果偏低;B.滴定终点时俯视读数,读数偏小,则消耗溶液的体积减少,测定结果偏高;C.锥形瓶用蒸馏水润洗,不影响实验结果;D.滴定管尖嘴处滴定前无气泡,滴定终点发现气泡,则消耗溶液的体积减少,则测定结果偏高;E.滴定时震荡锥形瓶较剧烈,则生成的碘离子被空气氧化生成单质碘,从而消耗溶液的体积增加,实验测定结果偏低,答案选AE。
考点:考查仪器识别、抽滤操作、反应条件的选择与控制、物质含量测定的有关计算与误差分析


科目:高中化学 来源: 题型:实验题
用含有A12O3、SiO2和少量FeO·xFe2O3的铝灰制备A12(SO4)3·18H2O,工艺流程如下(部分操作和条件略)
Ⅰ.向铝灰中加入过量稀H2SO4,过滤:
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
(1)H2SO4溶解A12O3的离子方程式是
(2)KMnO4氧化Fe2+的离子方程式补充完整:
(3)已知:生成氢氧化物沉淀的pH
| | Al(OH)3 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
碘是人体必需的元素之一,海洋植物如海带、海藻中含有丰富的、以化合态形式存在的碘元素。在实验室中,从海藻里提取碘的流程和实验装置如下: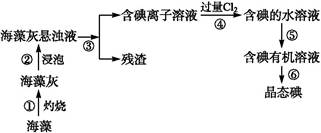
(1)指出上述提取碘的过程中有关实验操作的名称:步骤③ ,步骤⑤ 。
(2)写出步骤④对应反应的离子方程式: 。
(3)提取碘的过程中,可供选择的有机试剂是 。(填编号)
A.酒精 B.醋酸 C.四氯化碳 D.苯
(4)步骤④除了加入过量Cl2,下列氧化剂最好选用 (填代号)。
A.浓硫酸 B.H2O2溶液 C.KMnO4溶液
理由是____________________________。
(5)为了使海藻灰中的碘离子转化为碘的有机溶液,即完成步骤③至⑤,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器和物品,尚缺少的玻璃仪器是 。
(6)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏。指出下图实验装置中存在的错误之处: 。 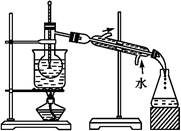
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某同学设计了如图所示装置进行石油分馏的实验。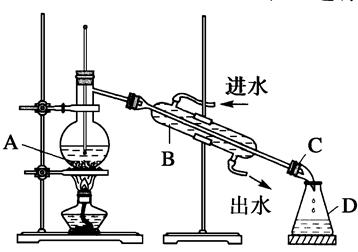
(1)指出实验装置中仪器A、B、C、D的名称:
A________、B________、C________、D________。
(2)指出该同学所设计的实验装置中存在的错误,并给予改正。
错误:①_______________________________________;
②_____________________________________________。
改正:①_______________________________________;
②_____________________________________________。
(3)实验装置改正后,进行气密性检查的方法:______________________________。
(4)蒸馏烧瓶中放入几片碎瓷片的作用是__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
溴乙烷是一种重要的化工合成原料。实验室合成溴乙烷的反应和实验装置如下:
反应:CH3CH2OH+HBr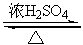 CH3CH2Br+H2O
CH3CH2Br+H2O
装置: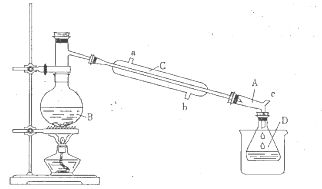
实验中可能用到的数据如下表:
| 物质 | 相对分子质量 | 沸点/℃ | 密度/g/cm3 | 水溶性 |
| CH3CH2OH | 46 | 78.4 | 0.79 | 互溶 |
| CH3CH2Br | 109 | 38.4 | 1.42 | 难溶 |
| CH3CH2OCH2CH3 | 74 | 34.5 | 0.71 | 微溶 |
| CH2=CH2 | 28 | -103.7 | 0.38 | 不溶 |
| 浓硫酸(H2SO4) | 98 | 338.0 | 1.38 | 易溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
菠菜营养丰富,长期以来民间流传着“菠菜不能与豆腐同食”的说法。某学校化学兴趣小组的同学拟通过实验探究:菠菜是否含有草酸类物质?草酸又有哪些性质?通过上网查询,获得以下资料:草酸又名乙二酸,其酸性比乙酸稍强,草酸及其盐具有较强的还原性,草酸晶体(H2C2O4·2H2O)的熔点为100.1℃,在175℃时受热分解,草酸钙是难溶于水的白色固体。
他们设计的实验步骤如下:
1.将菠菜在少量开水中煮沸2~3 min,冷却后滤去菠菜,得滤液(含有少量CO32—杂质)。向滤液中加入足量Ca(OH)2溶液,然后再加入足量CH3COOH溶液,观察现象。
2.用草酸晶体(H2C2O4·2H2O)做以下实验:
请回答以下问题:
(1)步骤1中加入CH3COOH溶液的作用:___________________
(2)A处应选择________(填“Ⅰ”或“Ⅱ”),在做实验之前,应先____________________。
(3)实验2过程中观察到C、E装置中的溶液均变浑浊,且D装置中黑色粉末变为红色,写出A中草酸晶体(H2C2O4·2H2O)发生反应的化学方程式:______________,装置B的作用是___________________。
(4)为使实验结论更加严密和安全,在以上所连接的装置C、D间还需依次添加装有________、________、________(液体试剂)的洗气瓶,此外指出上述装置中的不足之处还有________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某小组同学将一定浓度NaHCO3溶液加入到CuSO4溶液中发现生成了沉淀。甲同学认为沉淀是CuCO3;乙同学认为沉淀是CuCO3和Cu(OH)2的混合物,他们设计实验测定沉淀中CuCO3的质量分数。
(1)按照甲同学的观点,发生反应的离子方程式为 。
(2)两同学利用下图所示装置进行测定:
①在研究沉淀物组成前,须将沉淀从溶液中分离并净化。具体操作依次为过滤、洗涤、干燥。
②装置E中碱石灰的作用是 。
③实验过程中有以下操作步骤:
a.关闭K1、K3,打开K2、K4,充分反应
b.打开K1、K4,关闭K2、K3,通入过量空气
c.打开K1、K3,关闭K2、K4,通入过量空气
正确的顺序是 (填选项序号,下同)。若未进行步骤 ,将使测量结果偏低。
④若沉淀样品质量为m g,装置D质量增加了n g,则沉淀中CuCO3的质量分数为 。
(3)丙同学认为还可以通过测量CO2的体积并测量 来测定沉淀中CuCO3的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
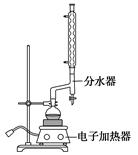
苯甲酸乙酯(C9H10O2)稍有水果气味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体、溶剂等。其制备方法为:
已知:
| | 颜色、状态 | 沸点(℃) | 密度(g·cm-3) |
| *苯甲酸 | 无色、片状晶体 | 249 | 1.2659 |
| 苯甲酸乙酯 | 无色澄清液体 | 212.6 | 1.05 |
| 乙醇 | 无色澄清液体 | 78.3 | 0.7893 |
| 环己烷 | 无色澄清液体 | 80.8 | 0.7318 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
如图1所示是实验室中制取气体的一种简易装置。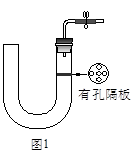
(1)请简述检验它的气密性的方法_______________________。
(2)利用如图1所示装置可以制取(填反应物状况及发生反应是否需要的条件)________________________气体。
某同学设计如图2所示装置,用粗铁粒与16.9%稀硝酸反应制取NO气体并探究产物中铁的价态。请回答有关问题。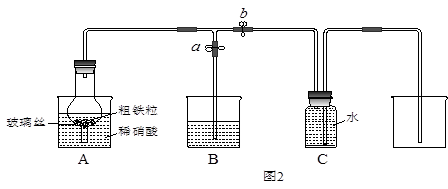
(3)已知16.9%稀硝酸的密度为1.10g/cm3,则其物质的量浓度为____________(计算结果保留两位小数)。用若用63%的硝酸配制16.9%稀硝酸500mL,所需的玻璃仪器有玻璃棒、烧杯和 。
(4)当打开止水夹a、关闭止水夹b时,A装置的干燥管中观察到的现象是_______________________。B装置烧杯中液体的作用是__________________________________。当A装置中气体几乎无色时,打开止水夹b,关闭止水夹a,可用C装置收集NO气体。
(5)已知下列反应可以发生:Fe2O3+3KNO3+4KOH 2K2FeO4+3KNO2+2H2O,而A装置中的稀硝酸即使换成浓硝酸,也不能生成+6价的铁的化合物,其原因是________。
2K2FeO4+3KNO2+2H2O,而A装置中的稀硝酸即使换成浓硝酸,也不能生成+6价的铁的化合物,其原因是________。
a.HNO3的氧化性比KNO3弱
b.反应的温度不够
c.HNO3的热稳定性比KNO3差
d.FeO42-不能存在于酸性溶液中
(6)现有仪器和药品:试管和胶头滴管,0.1mol/LKSCN溶液、0.2mol/L酸性KMnO4溶液、0.1mol/LKI溶液、氯水等。请你设计一个简单实验,探究A装置烧杯里完全反应后含铁可能的价态,填写下列实验报告:
| 实验步骤 | 操作 | 现象与结论 |
| 第一步 | 取少量液体装于试管,向试 管中滴入几滴KSCN溶液。 | |
| 第二步 | | 若溶液紫色褪去,则说明含有Fe2+; 若无明显变化,则说明不含Fe2+。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com