
| A. | 凡含有食品添加剂的食物对人体健康均有害 | |
| B. | 石油分馏、煤的气化、海水晒盐、碱去油污等过程都是化学变化 | |
| C. | 黄河入海口沙洲的形成与用卤水点豆腐,都体现了胶体聚沉的性质 | |
| D. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 |
分析 A.合理使用食品添加剂,对丰富食品生产和促进人体健康有好处;
B.石油分馏、海水晒盐没有新物质生成;
C.胶体遇电解质溶液发生聚沉;
D.聚酯纤维属于有机物.
解答 解:A.合理使用食品添加剂,对丰富食品生产和促进人体健康有好处,可以食用,但不能过量,故A错误;
B.石油分馏、海水晒盐没有新物质生成,属于化学变化,故B错误;
C.黄河中的泥沙和豆浆都是胶体,胶体遇电解质溶液发生聚沉,故C正确;
D.光导纤维的成分是二氧化硅,因制作航天服的聚酯纤维属于有机物,故D错误.
故选C.
点评 本题考查化学与环境、材料、信息、能源关系密切相关的知识,为高频考点,侧重于基础知识的综合理解和运用的考查,难度不大.


 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:选择题
| A. | CO2+H2O→H2CO3 | B. | H2+I2→HI | C. | NH3+HCl→NH4Cl | D. | SO2+O2→SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中氧化剂是CO、还原剂是NO2 | |
| B. | 该反应是氧化还原反应 | |
| C. | 该反应生成28 g N2时,转移8 mol e- | |
| D. | 该反应能减少汽车尾气对环境的污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铍原子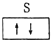 | B. | 碳原子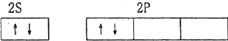 | ||
| C. | 氯原子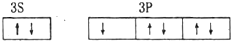 | D. | 铝原子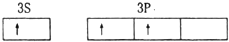 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
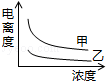 B.
B. C.
C.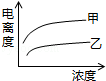 D.
D.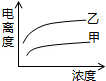
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1 4.3×10-7 K2 5.6×10-11 | 3.0×10-8 |
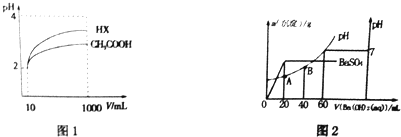
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
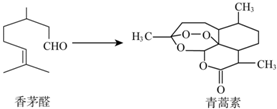
| A. | 香茅醛能使Br2的CCl4溶液褪色 | |
| B. | 青蒿素分子式为C15H22O5 | |
| C. | 青蒿素在一定条件下可发生水解反应 | |
| D. | 二者均可与氢气发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

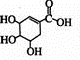 +Br2→
+Br2→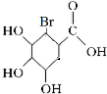 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4--天然气 | B. | CaO--熟石灰 | C. | Na2CO3--小苏打 | D. | NaHCO3--苏打粉 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com