
| A、加入催化剂,逆反应速率不变 |
| B、增大反应体系的压强,正反应速率一定增大 |
| C、升高温度,反应速率加快,反应放出的热量减小 |
| D、若在原电池中进行,反应放出的热量不变 |


 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:
| A、生铁的抗腐蚀能力比纯铁弱 |
| B、用锡焊接的铁质器件,焊接处易生锈 |
| C、将钢闸门与直流电源的正极相连可防止其被腐蚀 |
| D、轮船外壳在海水中锈蚀的主要原因是发生吸氧腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3COONa |
| B、NaCl |
| C、Na2CO3 |
| D、NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
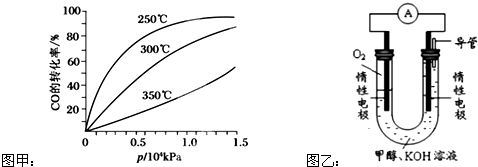
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、处于最低能量的原子叫做基态原子 |
| B、原子由基态变为激发态要产生发射光谱 |
| C、同一原子中,2p能级比3p能级的轨道数少 |
| D、3d轨道能量小于4s |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
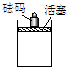 在一定条件下,向如图容器中加入一定量的A和B,发生反应:mA+nB?pC达到平衡.
在一定条件下,向如图容器中加入一定量的A和B,发生反应:mA+nB?pC达到平衡.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com