
已知:H2O(g)===H2O(l) ΔH=Q1 kJ·mol-1
C2H5OH(g)===C2H5OH(l) ΔH=Q2 kJ·mol-1
C2H5OH(g)+3O2(g)===2CO2(g)+3H2O(g) ΔH=Q3 kJ·mol-1
若使46 g酒精液体完全燃烧,最后恢复到室温,则放出的热量为( )
A.(Q1+Q2+Q3) kJ B.0.5(Q1+Q2+Q3) kJ
C.(0.5Q1-1.5Q2+0.5Q3) kJ D.-(3Q1-Q2+Q3) kJ
科目:高中化学 来源: 题型:
某有机物完全燃烧时只生成水和二氧化碳,且两者的物质的量之比为3∶2,则( )
A.该有机物含碳.氢.氧三种元素 B.该化合物是乙烷
C.该化合物分子中碳.氢原子个数之比是2∶3
D.该有机物含2个碳原子,6个氢原子,但不能确定是否含氧原子
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物A由碳、氢、氧三种元素组成。现取2.3 g A与2.8 L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过浓硫酸和碱石灰, 浓硫酸增重2.7 g, 碱石灰增重2.2 g。回答下列问题:
(1)2.3 g A中所含氢原子、碳原子的物质的量各是多少?
(2)通过计算确定该有机物的分子式。
查看答案和解析>>
科目:高中化学 来源: 题型:
向_FeCl3、Al2(SO4)3的混和溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情况如下图所示。沉淀的生成与溶解的pH列于下表(已知:偏铝酸钡易溶于水).以下推断正确的是
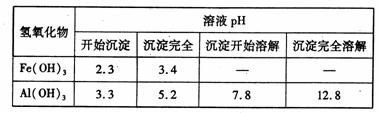
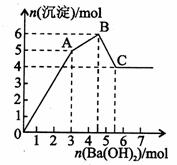
A.据图计算原溶液中c(Cl一)=c(SO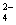 )
)
C.OA段产生的沉淀为BaSO4和Fe(OH)3
B.AB段可能发生的反应是:2SO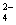 +2Ba2++ Al3+ +30H-= 2BaSO4k +Al(OH)3↓
+2Ba2++ Al3+ +30H-= 2BaSO4k +Al(OH)3↓
D.C点溶液呈碱性的原因是AlO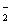 水解,其离子方程式为:AlO
水解,其离子方程式为:AlO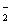 +2H2O=Al(OH)3 +OH一
+2H2O=Al(OH)3 +OH一
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃、100 kPa条件下:
4Al(s)+3O2(g)===2Al2O3(s) ΔH=-2 834.9 kJ·mol-1
4Al(s)+2O3(g)===2Al2O3(s) ΔH=-3 119.1 kJ·mol-1
由此得出的正确结论是( )
A.等质量的O2比O3能量低,由O2变为O3为吸热反应
B.等质量的O2比O3能量低,由O2变为O3为放热反应
C.O3比O2稳定,由O2变为O3为吸热反应
D.O2比O3稳定,由O2变为O3为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
将煤转化为水煤气的主要化学反应为C(s)+H2O(g)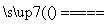 CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:
CO(g)+H2(g);C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:
C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
H2(g)+ O2(g)===H2O(g) ΔH=-242.0 kJ·mol-1
O2(g)===H2O(g) ΔH=-242.0 kJ·mol-1
CO(g)+ O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
请回答:
(1)根据以上数据,写出C(s)与水蒸气反应的热化学反应方程式:________________________________________________________________________。
(2)比较反应热数据可知,1 mol CO(g)和1 mol H2(g)完全燃烧放出的热量之和比1 mol C(s)完全燃烧放出的热量多。甲同学据此认为“煤转化为水煤气可以使煤燃烧放出更多的热量”;乙同学根据盖斯定律做出下列循环图:
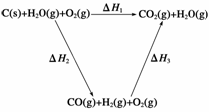
并据此认为“煤转化为水煤气再燃烧放出的热量与煤直接燃烧放出的热量相等”。
请分析:甲、乙两同学观点正确的是__________(填“甲”或“乙”);判断的理由是________________________________________________________________________
________________________________________________________________________。
(3)将煤转化为水煤气作为燃料和煤直接燃烧相比有很多优点,请列举其中的两个优点:________________________________________________________________________
________________________________________________________________________。
(4)水煤气不仅是优良的气体燃料,也是重要的有机化工原料。CO和H2在一定条件下可以合成:①甲醇 ②甲醛 ③甲酸 ④乙酸。试分析当CO和H2按1∶1的体积比混合反应,合成上述________(填序号)物质时,可以满足“绿色化学”的要求,完全利用原料中的原子,实现零排放。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生活、社会密切相关。下列说法不正确的是 ( )。
A.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境
B.凡含有食品添加剂的食物对人体健康均有害,不可食用
C.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
D.提倡人们购物时不用塑料袋,是为了防止白色污染
查看答案和解析>>
科目:高中化学 来源: 题型:
蛋白质是生命的基础,没有蛋白质就没有生命。请回答下列问题:
(1)蛋白质分子中含有________、__________、__________________、
__________四种元素,有的还含有________等元素;
(2)蛋白质的基本组成单位是氨基酸,天然氨基酸通式为__________________________________________________________________
________________________________________________________________________。
(3)人体摄入的蛋白质在胃蛋白酶和胰蛋白酶的作用下,水解成________,被人体吸收后,重新结合成人体所需的蛋白质。人体内蛋白质也在不断分解,最后生成尿素排出体外。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com