
【题目】使反应4NH3(g)+3O2(g)=2N2(g)+6H2O(g)在2 L的密闭容器中进行,半分钟后N2的物质的量增加了0.60 mol。则下列选项中反应的平均速率正确的为
A.v(O2)=0.90 mol·L-1·min-1B.v(NH3)=0.04 mol·L-1·s-1
C.v(N2)=0.02 mol·L-1·s-1D.v(H2O)=1.20 mol·L-1·min-1
科目:高中化学 来源: 题型:
【题目】常温下 ,向 20.00mL 0. 1molL-1 BOH溶液中 滴入 0. 1 mo lL-1 盐酸 ,溶液中由水电离出的 c ( H+ ) 的负对数 [ - l gc水( H+ ) ] 与所加盐酸体积的关系如下图所示,下列说法正确的是
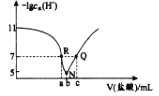
A.常温下,BOH的电离常数约为 1×10-4
B.N 点溶液离子浓度顺序:c(B+)>c(Cl-)> c( OH- )>c( H+)
C.a =20
D.溶液的pH: R > Q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从溴乙烷制取1,2-二溴乙烷,下列制备方案中最好的是( )
A. CH3CH2Br![]() CH3CH2OH
CH3CH2OH![]() CH2=CH2
CH2=CH2![]() CH2BrCH2Br
CH2BrCH2Br
B. CH3CH2Br![]() CH2BrCH2Br
CH2BrCH2Br
C. CH3CH2Br![]() CH2=CH2
CH2=CH2![]() CH3CH2Br
CH3CH2Br![]() CH2BrCH2Br
CH2BrCH2Br
D. CH3CH2Br![]() CH2=CH2
CH2=CH2![]() CH2BrCH2Br
CH2BrCH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10 mL0.1 mol/L的HR溶液中逐滴加入0.1 mol/L的氨水,所得溶液pH及导电能力变化如图。下列分析正确的是( )
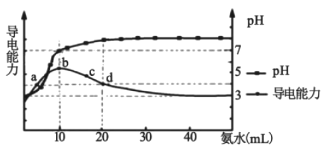
A. 各点溶液中的阳离子浓度总和大小关系:d>c>b>a
B. 常温下,R- 的水解平衡常数数量级为10 -9
C. a点和d点溶液中,水的电离程度相等
D. d点的溶液中,微粒浓度关系:c(R-)+2c(HR)=c(NH3H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是
A.25℃时 pH=2 的 HF 溶液中,由水电离产生的 OH-浓度为 10-12 mol·L-1
B.0.1 mol·L-1 Na2CO3 溶液中:c(Na+)=c(HCO3 -)+c(H2CO3)+2c(CO32- )
C.向 1 L 1 mol·L-1 的 NaOH 热溶液中通入一定量 Br2,恰好完全反应生成溴化钠、次溴酸钠和溴酸钠(溴 酸为强酸、次溴酸为弱酸)的混合溶液:c(Na+)+c(H+)=6c(BrO3-)+2c(BrO-)+c(HBrO)+c(OH-)
D.25℃时 pH=3 的盐酸与 pH=11 的氨水等体积混合,所得溶液的 pH<7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.对于乙酸与乙醇的酯化反应(ΔH<0),加入少量浓硫酸并加热,该反应的反应速率与平衡常数均增大
B.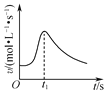 如图是镁条与盐酸反应的化学反应速率随反应时间变化的曲线,说明t1时刻溶液的温度最高
如图是镁条与盐酸反应的化学反应速率随反应时间变化的曲线,说明t1时刻溶液的温度最高
C.反应2HI(g)H2(g)+I2(g),达到平衡后,缩小容器容积可使体系颜色变深。该现象不能用勒夏特列原理解释
D.若反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)在常温下能自发进行,则该反应的ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近日,我国科研团队研发出一种蓝藻人造叶片系统,其核心是一种可以向细胞外分泌蔗糖的蓝藻,其工作原理如图。下列说法不正确的是
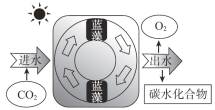
A. 该系统利用了蓝藻的光合作用
B. 理论上,系统出水量小于进水量
C. 可用银氨溶液检验产物中是否含蔗糖
D. 该系统有望为人类探索太空时解决生存难题提供新思路
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 2Na + 2H2O = 2NaOH + H2↑,该反应中相关物质的化学用语中正确的是
A.H2 的结构式:H-H
B.中子数为 12 的钠原子:![]()
C.H2O 的电子式:![]()
D.Na+的结构示意图:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com