
| A.通入Ca(ClO)2溶液中,有HClO生成 | B.通入FeCl3溶液中,有SO42-生成 |
| C.通入氯水中,有淡黄色沉淀生成 | D.通入KICl2溶液中,有I-生成 |


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源:不详 题型:单选题
| A.①⑤ | B.②③④ | C.全部 | D.都不是 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.高沸点性; | B.酸性; | C.吸水性; | D.脱水性;(E)强氧化性。试用字母填空: |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
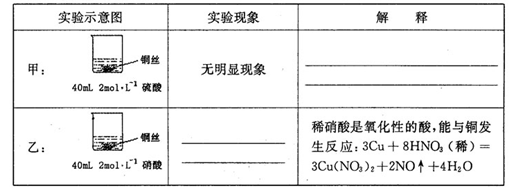
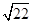 =0.7)
=0.7)查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
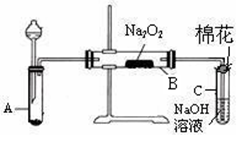
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
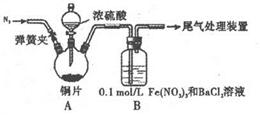
| A.将产生的气体缓缓通过预先称量的盛有碱石灰的干燥管,结束反应后再次称貴 |
| B.将产生的气体缓缓通入酸性髙锰酸钾溶液,再加入足量BaCl2溶液,过滤、洗涤、干燥、称量沉淀 |
| C.用排水法测定其产生气体的体积(折算成标准状况) |
| D.用排饱和NaHSO3溶液的方法测定其产生气体的体积(折算成标准状况) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.通常条件下都是无色气体,易溶于水 | B.都是酸性氧化物,其水溶液都是强酸 |
| C.都可使品红溶液褪色,加热时红色又能再现 | D.都能与碱溶液反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.二氧化硫具有漂白性 | B.溴挥发而褪色 |
| C.二氧化硫具有还原性 | D.溴被还原成Br— |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com