
在CO、CO2、SO2、NO、NO2、SiO2等氧化物中:
①其中属于酸性氧化物的是________,能形成酸雨的是__________________;
②能与水发生氧化还原反应的是______________,反应的化学方程式为
________________________________________________________________________;
③能使品红溶液褪色的是__________;
④光导纤维的主要成分是________,它与氢氟酸、烧碱反应的化学方程式分别为
______________,____________________________________________________________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列有关化学键的叙述,正确的是( )
A.非金属元素组成的化合物中只含共价键
B.水溶液能导电的化合物一定是离子化合物
C.化合物MgO、SiO2、 SO3中化学键的类型相同
D.PH3分子稳定性低于NH3分子,因为N—H键键能高
查看答案和解析>>
科目:高中化学 来源: 题型:
一定能在下列溶液中大量共存的离子组是( )
A.含有大量Al3+的溶液:Na+、NH 、SO
、SO 、Cl-
、Cl-
B.c(H+)=1×10-13 mol·L-1的溶液:Na+、Ca2+、SO 、CO
、CO
C.含有大量Fe3+的溶液:Na+、Mg2+、NO 、SCN-
、SCN-
D.含有大量NO 的溶液:H+、Fe2+、SO
的溶液:H+、Fe2+、SO 、Cl-
、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
阿伏加德罗常数的值约为6.02×1023,下列叙述正确的是( )
A.4 g重水(D2O)中所含质子数为2×6.02×1023
B.磷酸的相对分子质量与6.02×1023个磷酸分子的质量相等
C.25℃,pH=13的NaOH溶液中含有OH-数约为6.02×1022
D.6.02×1022个氯气分子溶于水形成1 000 mL溶液,溶液中c(Cl-)=0.1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.硅晶体中,有NA个Si就有2NA个Si—Si键
B.同温同压下,相同体积的氟气和氩气所含的原子数相等
C.1 mol CnH2n中含有的共用电子对数为(3n+1)NA
D.在含2 mol H2SO4的浓硫酸中加入足量的Zn粉,充分反应后转移电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列与实验相关的叙述正确的是(双选)( )
A.稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中
B.将SO2和Cl2按等物质的量比通入品红溶液中,品红溶液不褪色
C.NO2与H2O反应的过程中,被氧化的氮原子与被还原的氮原子的个数比为2∶1
D.因为NH3·H2O是弱碱,所以不能用氨水与FeCl3溶液反应制取Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
用下图所示的实验装置A加热AgNO3固体,产生红棕色气体,在装置D中收集到无色气体。经小组讨论并验证无色气体为O2,其验证方法是________________________________________________________________________。

(2)[2013·海南17(1)改编]BaCl2·xH2O中结晶水数目可通过重量法来确定;①称取样品,置于小烧杯中,加入适量稀盐酸,加热溶解,边搅拌边滴加稀硫酸到沉淀完全,静置;②过滤并洗涤沉淀;③……
在操作②中,需要先后用稀硫酸和________洗涤沉淀;检验沉淀中氯离子是否洗净的方法是________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
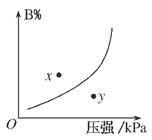
反应mA(s)+nB(g)⇌pC(g)ΔH<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是( )
①m+n>p; ②x点表示的正反应速率大于逆反应速率;
③n>p; ④x点比y点时的反应速率慢;
⑤若升高温度,该反应的平衡常数增大。
A.①②⑤ B.只有②④ C.只有①③ D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是1 mol NO2g)和1 mol COg)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,则E1________填“增大”、“减小”或“不变”,下同),ΔH________。
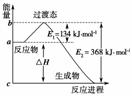
请写出NO2和CO反应的热化学方程式:
____________________________________________________。
2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OHg)+H2Og)===CO2g)+3H2g)
ΔH=+49.0 kJ·mol-1
②CH3OHg)+1/2O2g)===CO2g)+2H2g)
ΔH=-192.9 kJ·mol-1。
又知③H2Og)===H2Ol) ΔH=-44 kJ·mol-1
则甲醇蒸气完全燃烧生成液态水的热化学方程式为
____________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com