
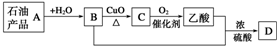
| A. | A能使酸性高锰酸钾溶液褪色 | B. | 可用B萃取碘水中的碘单质 | ||
| C. | B与乙酸发生了取代反应 | D. | D的结构简式为CH3COOCH2CH3 |
分析 A和水反应生成B,B能发生氧化反应生成C,C发生催化氧化生成乙酸,则C为CH3CHO、B为CH3CH2OH、A为
CH2=CH2,在浓硫酸作催化剂、加热条件下,乙醇和乙酸发生酯化反应生成D,D为CH3COOCH2CH3,结合题目分析解答.
解答 解:A和水反应生成B,B能发生氧化反应生成C,C发生催化氧化生成乙酸,则C为CH3CHO、B为CH3CH2OH、A为CH2=CH2,在浓硫酸作催化剂、加热条件下,乙醇和乙酸发生酯化反应生成D,D为CH3COOCH2CH3,
A.A为乙烯,乙烯中含有碳碳双键,性质较活泼,能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,故A正确;
B.B为乙醇,乙醇和水互溶,所以乙醇不能萃取碘水中的碘,故B错误;
C.乙醇和乙酸的酯化反应也属于取代反应,故C正确;
D.通过以上分析知,D结构简式为CH3COOCH2CH3,故D正确;
故选B.
点评 本题考查有机物结构和性质,为高频考点,侧重考查学生分析判断能力,明确烯烃、醇、醛、羧酸、酯之间的相互转化是解本题关键,熟悉常见官能团及其性质,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 互为同分异构体 | B. | 最简式相同 | ||
| C. | 互为为同系物 | D. | 每个烃分子含相同数目的碳原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 部分难溶物的颜色和常温下的Ksp如下表所示:
部分难溶物的颜色和常温下的Ksp如下表所示:| Cu(OH)2 | CuOH | CuCl | Cu2O | |
| 颜色 | 蓝色 | 黄色 | 白色 | 砖红色 |
| Ksp(25℃) | 1.6×10-19 | 1.0×10-14 | 1.2×10-6 | - |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为防止铁生锈,在其表面涂一层防锈油漆 | |
| B. | 为防止火灾,在面粉厂、加油站等场所要严禁烟火 | |
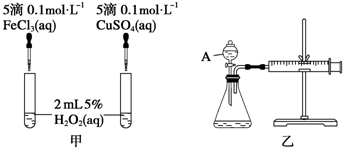
| C. | 为加快H2O2的分解速率,把反应容器放到冷水中冷却 | |
| D. | 为加快KClO3的分解速率,加入MnO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向0.10mol•L-1NH4HCO3溶液中通入CO2:c(NH4+)=c(HCO3-)+c(CO32-) | |
| B. | 0.10mol•L-1CH3COONa溶液中通入HCl:c(Na+)>c(Cl-)>c(CH3COOH) | |
| C. | 0.10mol•L-1Na2SO3溶液通入SO2:c(Na+)=2[c(SO32-)+c(HSO3-)+c(H2SO3)] | |
| D. | 向0.10mol•L-1NaHSO3溶液中通入NH3:c(Na+)>c(SO32-)>c(NH4+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com