
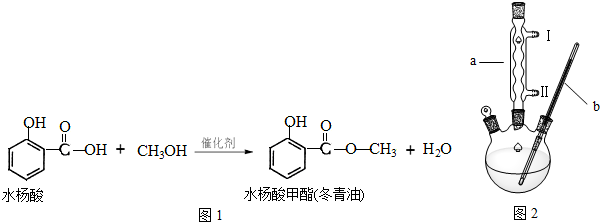
| 实际量 |
| 理论量 |
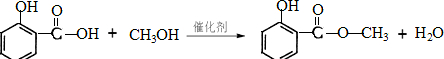
| 实际量 |
| 理论量 |
| 6.8g |
| 7.6g |


科目:高中化学 来源: 题型:
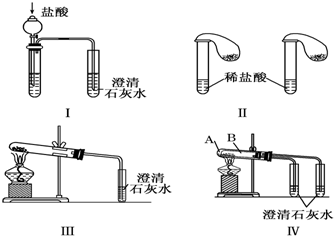
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、11.2 g Fe投入到400mL 1mol/L的硝酸中充分反应,转移电子总数为0.2NA |
| B、标准状况下,11.2LC2H6含3NA个C-H极性共价键 |
| C、标准状况下,5.6LNO和5.6LO2混合后的分子总数为0.5NA |
| D、标准状况下,铝跟氢氧化钠溶液反应生成1 mol氢气时,转移的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,16gO2与O3的混合气体中含氧原子数为NA |
| B、0.05mol硫酸氢钠晶体中含离子总数为0.15NA |
| C、标准状况下,22.4LCCl4中含有氯原子数目为4NA |
| D、一定条件下,2mol二氧化硫和1 mol氧气混合,反应时转移的电子数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
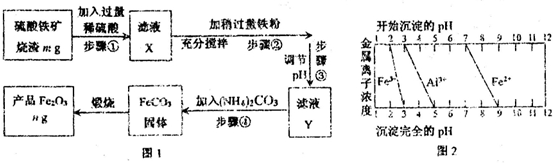
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向某溶液中加入新制氯水和CCl4,振荡、静置,若下层显紫色,证明原溶液中存在I- |
| B、某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+ |
| C、向某溶液中先加入新制氯水,再加入KSCN溶液,若溶液呈血红色,证明含有Fe2+ |
| D、加入盐酸,能产生使澄清石灰水变浑浊的气体,则溶液中一定含有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
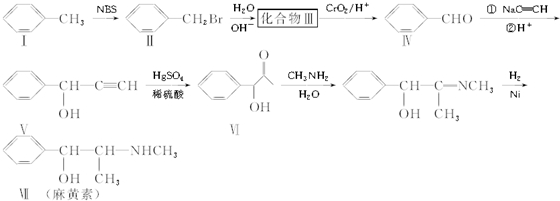
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、根据金属活动性顺序表,可以推断冶炼金属时可能的方法 |
| B、CaCl2、MgCl2晶体都容易潮解,它们潮解的实质是晶体表面吸水形成溶液 |
| C、根据某元素原子的质子数和中子数,可以确定该元素的相对原子质量 |
| D、根据酸、碱、盐的溶解性表,可以判断某些溶液中的复分解反应能否进行 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com