
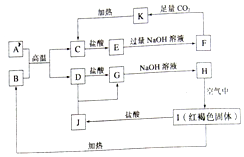
分析 红褐色固体I为Fe(OH)3,则B为Fe2O3,A是铝,且A+B→C+D是置换反应,D系列转化得到氢氧化铁,则D为Fe,C为Al2O3,可推知G为FeCl2、H为Fe(OH)2、J为FeCl3,E为AlCl3,F为NaAlO2、K为Al(OH)3,据此解答.
解答 解:红褐色固体I为Fe(OH)3,则B为Fe2O3,A是铝,且A+B→C+D是置换反应,D系列转化得到氢氧化铁,则D为Fe,C为Al2O3,可推知G为FeCl2、H为Fe(OH)2、J为FeCl3,E为AlCl3,F为NaAlO2、K为Al(OH)3.
(1)B为Fe2O3,可以用作油漆颜料,故答案为:油漆颜料;
(2)A+B→C+D的反应方程式为:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,
H→I的反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3;4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)D+J→G的离子方程式为:2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe=3Fe2+;
(4)检验FeCl3中阳离子的方法是:取少量溶液于小试管中,滴加几滴KSCN溶液,若溶液出现红色,说明含有Fe3+,
故答案为:取少量溶液于小试管中,滴加几滴KSCN溶液,若溶液出现红色,说明含有Fe3+.
点评 本题考查无机物推断,涉及Al、Fe元素单质化合物的性质,物质的颜色是推断突破口,注意对基础知识的掌握,难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
 X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示.下列说法错误的是( )
X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示.下列说法错误的是( )| A. | Q位于第三周期IA族 | |
| B. | X、Y、Z三种元素组成的化合物可能是盐或碱 | |
| C. | 简单离子半径:M->Q+>R2+ | |
| D. | Z与M的最高价氧化物对应水化物均为强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠溶液盛装在用玻璃塞的试剂瓶中 | |
| B. | 氢氟酸盛装在玻璃瓶中 | |
| C. | 金属钠保存在煤油中 | |
| D. | 硝酸银固体存放在细口瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同物质的量的石墨与金刚石相比,金刚石的总能量更高 | |
| B. | 金刚石转化为石墨是放热反应,金刚石比石墨稳定 | |
| C. | 金刚石转化为石墨是吸热反应,石墨比金刚石稳定 | |
| D. | 两者互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液浓度相等 | |
| B. | c(Cl-)=c(CH3COO-) | |
| C. | 等体积的两种酸,中和所需NaOH溶液的体积盐酸比醋酸多 | |
| D. | 分别加水稀释至原体积的10倍,盐酸的pH小于醋酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2和NO | B. | NO2和CO2 | C. | N2和O2 | D. | O2和CO |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com