
【题目】金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:WO3 (s) + 3H2 (g) ![]() W (s) + 3H2O (g) 请回答下列问题:
W (s) + 3H2O (g) 请回答下列问题:
(1)上述反应的化学平衡常数表达式为___________________________。
(2) 某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为_______;随温度的升高,H2与水蒸气的体积比减小,则该反应为___________反应(填“吸热”或“放热”)。
(3)上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
温度 | 25℃ 550℃ 600℃ 700℃ |
主要成份 | WO3 W2O5 WO2 W |
第一阶段反应的化学方程式为________;580℃时,固体物质的主要成分为________;假设WO3完全转化为W,则三个阶段消耗H2物质的量之比为__________________。
(4)已知:温度过高时,WO2 (s)转变为WO2 (g);
WO2 (s) + 2H2 (g) ![]() W (s) + 2H2O (g);ΔH = +66.0 kJ·mol-1
W (s) + 2H2O (g);ΔH = +66.0 kJ·mol-1
WO2 (g) + 2H2 ![]() W (s) + 2H2O (g);ΔH = -137.9 kJ·mol-1
W (s) + 2H2O (g);ΔH = -137.9 kJ·mol-1
则WO2 (s) ![]() WO2 (g) 的ΔH = ______________________。
WO2 (g) 的ΔH = ______________________。
(5)钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W (s) +2I2 (g) ![]() WI4 (g)。下列说法正确的有________。
WI4 (g)。下列说法正确的有________。
a.灯管内的I2可循环使用
b.WI4在灯丝上分解,产生的W又沉积在灯丝上
c.WI4在灯管壁上分解,使灯管的寿命延长
d.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢
【答案】 ![]() 60%吸热2WO3 + H2
60%吸热2WO3 + H2 ![]() W2O5 + H2OW2O5、WO21:1:4+203.9 kJ·mol-1 a、b
W2O5 + H2OW2O5、WO21:1:4+203.9 kJ·mol-1 a、b
【解析】
化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,据此书写,注意固体、纯液体不需要写出;由反应方程式知,消耗的H2与生成的水的物质的量相等,假定H2与水蒸气的物质的量分别为3mol、5mol,再根据转化率定义计算;500℃时,温度介于25℃~550℃,固体为WO3;由表中主要成分与温度关系可知,第二阶段反应为W2O5与H2反应生成WO2,同时还生成H2O,配平书写方程式;根据三个阶段的方程式进行计算三个阶段消耗H2物质的量之比;由化学方程式知,挥发的W与I2结合形成气态WI4,由于气体运动的结果,WI4会与还没有挥发的W接触,在高温下WI4分解生成的W附着在还没有挥发的W上,灯管壁温度较低,WI4不会分解,升高温度,正逆反应速率都加快,据此解答。
(1)WO3(s)+3H2(g)![]() W(s)+3H2O(g)的平衡常数k=
W(s)+3H2O(g)的平衡常数k=![]() ;(2)由反应方程式知,消耗的H2与生成的水的物质的量相等,故H2的平衡转化率为
;(2)由反应方程式知,消耗的H2与生成的水的物质的量相等,故H2的平衡转化率为![]() ×100%=60%,升高温度,H2与水蒸气的体积比减小,说明升温时平衡向右移动,故正反应为吸热反应;(3)由表中主要成分与温度关系可知,第一阶段反应为WO3与H2反应是W2O5,同时还生成H2O,反应方程式为:2WO3+H2
×100%=60%,升高温度,H2与水蒸气的体积比减小,说明升温时平衡向右移动,故正反应为吸热反应;(3)由表中主要成分与温度关系可知,第一阶段反应为WO3与H2反应是W2O5,同时还生成H2O,反应方程式为:2WO3+H2 ![]() W2O5+H2O,580℃时,温度介于550℃~600℃,固体为W2O5、WO2的混合物;假定有2molWO3,由2WO3+H2
W2O5+H2O,580℃时,温度介于550℃~600℃,固体为W2O5、WO2的混合物;假定有2molWO3,由2WO3+H2 ![]() W2O5+H2O、W2O5+H2
W2O5+H2O、W2O5+H2 ![]() 2WO2+H2O、WO2+2H2
2WO2+H2O、WO2+2H2 ![]() W+2H2O可知,三个阶段消耗的氢气的物质的量之比为1mol:1mol:2mol×2=1:1:4;(4)已知:①WO2(s)+2H2(g)W(s)+2H2O(g)△H=+66.0kJmol-1,②WO2(g)+2H2W(s)+2H2O(g)△H=-137.9kJmol-1,依据盖斯定律,①-②得WO2(s)WO2(g),故△H=66.0kJmol-1-(-137.9kJmol-1)=+203.9 kJmol-1;(5)由所给化学方程式知,挥发的W与I2结合形成气态WI4,由于气体运动的结果,WI4会与还没有挥发的W接触,在高温下WI4分解生成的W及I2,生成W附着在还没有挥发的W上,灯管内的I2可循环使用,故a、b对;灯管壁温度较低,WI4不会分解,故c错;升高温度,也能加快W与I2的反应速率,故d错,答案选ab。
W+2H2O可知,三个阶段消耗的氢气的物质的量之比为1mol:1mol:2mol×2=1:1:4;(4)已知:①WO2(s)+2H2(g)W(s)+2H2O(g)△H=+66.0kJmol-1,②WO2(g)+2H2W(s)+2H2O(g)△H=-137.9kJmol-1,依据盖斯定律,①-②得WO2(s)WO2(g),故△H=66.0kJmol-1-(-137.9kJmol-1)=+203.9 kJmol-1;(5)由所给化学方程式知,挥发的W与I2结合形成气态WI4,由于气体运动的结果,WI4会与还没有挥发的W接触,在高温下WI4分解生成的W及I2,生成W附着在还没有挥发的W上,灯管内的I2可循环使用,故a、b对;灯管壁温度较低,WI4不会分解,故c错;升高温度,也能加快W与I2的反应速率,故d错,答案选ab。


科目:高中化学 来源: 题型:
【题目】(14分)按要求完成下列填空
Ⅰ.已知:①2C3H8(g)+7O2(g)=6CO(g)+8H2O(l) ΔH=-2741.8kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH="-566" kJ/mol
(1)反应C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)的ΔH= ;
(2)C3H8在不足量的氧气里燃烧,生成CO和CO2以及气态水,将所有的产物通入一个固定体积的密闭容器中,在一定条件下发生如下可逆反应:CO(g)+ H2O(g)![]() CO2(g)+ H2(g) ΔH>0
CO2(g)+ H2(g) ΔH>0
①下列事实能说明该反应达到平衡的是 ;
a.体系中的压强不发生变化
b.υ正(H2)=υ逆(CO)
c.混合气体的平均相对分子质量不发生变化
d.CO2的浓度不再发生变化
②在某温度下,反应物的起始浓度分别为:c(CO)=" 1" mol·L-1, c(H2O)="2.4" mol·L-1; 达到平衡后,CO的转化率为60%,该反应在此温度下的平衡常数是 ;
(3)熔融碳酸盐燃料电池的电解质为Li2CO3和 Na2CO3的混合物,燃料为CO,在工作过程中,电解质熔融液的组成、浓度都不变,写出负极发生的电极反应式 。
Ⅱ.氮化硅(Si3N4)是一种新型陶瓷材料,它可用石英与焦炭在高温的氮气流中反应制得:
SiO2 + C + N2![]() Si3N4 + CO 根据题意完成下列各题:
Si3N4 + CO 根据题意完成下列各题:
(1)配平上述化学反应方程式。 SiO2 + C + N2![]() Si3N4 + CO
Si3N4 + CO
(2)为了保证石英和焦炭尽可能的转化,氮气要适当过量。某次反应用了30mol氮气,反应生成了5mol一氧化碳,则此时混合气体的平均摩尔质量是 。
(3)氮化硅陶瓷的机械强度高,硬度接近于刚玉(A12O3),热稳定性好,化学性质稳定。以下用途正确的是 。
A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备 |
B.在电子工业上制成耐高温的电的良导体 |
C.研发氮化硅的全陶发动机替代同类型金属发动机 |
D.氮化硅陶瓷的开发受到资源的限制,没有发展前途 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积恒定的密闭容器中,一定量的SO2与1.100molO2在催化剂作用下加热到600℃发生反应:2SO2+ O2![]() 2SO3,ΔH<0。当气体的物质的量减少0.315mol时反应达到平衡,在相同温度下测得气体压强为反应前的82.5%。下列有关叙述正确的是
2SO3,ΔH<0。当气体的物质的量减少0.315mol时反应达到平衡,在相同温度下测得气体压强为反应前的82.5%。下列有关叙述正确的是
A. 当SO3的生成速率与SO2的消耗速率相等时反应达到平衡
B. 降低温度,正反应速率减小程度比逆反应速率减小程度大
C. 将平衡混合气体通入过量BaCl2溶液中,得到沉淀的质量为161.980g
D. 达到平衡时,SO2的转化率为90%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求写出下列化学方程式或离子方程式:
(1)硫酸酸化的高锰酸钾与草酸反应的化学方程式:_____________________________。
(2)硫代硫酸钠与稀硫酸反应的化学方程式:____________________________________。
(3)硫酸酸化的碘化钾溶液与氧气反应的离子方程式:________________________。
(4)K2Cr2O7的溶液中K2Cr2O7与K2CrO4转化的离子方程式:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在CH3COOH溶液中存在如下平衡:CH3COOHH++CH3COO-。加入少量下列物质或采取下述方法,能使平衡逆向移动的是
A.加水B.CH3COONa固体C.升温D.NaCl固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从精炼钢的阳极泥中(主要成分为Cu2Te)回收碲的工艺流程如下:

请回答下列问题:
(1)“焙烧”后,碲主要以TeO2形式存在,则每生成32gTeO2,反应转移电子的物质的量为____________mol。
(2)为选择最佳焙烧工艺,进行温度和硫酸加入量的条件试验,结果如下表所示:
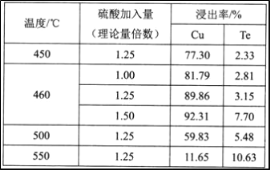
则实验中应选择的条件为________________________。
(3)“氧化”时的溶液温度不宜过高,原因为________________________。
(4)工艺(I)中,“还原”时发生的总离子方程式为______________________________。H2SO4和Na2SO3可用浓盐酸代替,但缺点为______________________________________。
(5)工艺(II)中,“浸出液电积”时产生碲粉的电极反应式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.Na在氧气中燃烧主要生成Na2O
B.将SO2通入BaCl2溶液可生成BaSO3沉淀
C.将CO2通入次氯酸钙溶液可生成次氯酸
D.将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)一定量的浓硝酸与足量铜完全反应,得到硝酸铜溶液和NO2、NO的混合气体2.24L(标准状况),这些气体与一定体积的O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入4mol.L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是50mL,下列说法正确的是
A. 参加反应的硝酸是0.4mol B. 消耗氧气的体积为1.68L
C. 混合气体中含NO2 1.12L D. 此反应过程中转移的电子为0.3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2O2是一种常见的过氧化物,具有强氧化性和漂白性。 通常可用作漂白剂和呼吸面具中的供氧剂。
(1)某实验小组通过下列实验探究过氧化钠与水的反应:

①用化学方程式解释使酚酞试液变红的原因___________________,依据实验现象推测红色褪去的原因是________________。
②加入MnO2的作用为_______________________。
(2)某实验小组拟验证CO2与Na2O2反应的产物,现设计以下实验装置进行实验:


①写出装置A中反应的化学方程式____________________;
②拟用装置D收集气体产物,请在方框中将装置补充完整______。
③产物检验:检验气体产物的方法:___________________;
④有同学认为该实验装置存在明显缺陷,你认为该缺陷是什么____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com