
| A. | 次氯酸分子的结构式: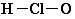 | |
| B. | 质量数为37的氯原子:${\;}_{37}^{17}$Cl | |
| C. | NH4Cl的电子式: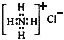 | |
| D. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O |
分析 A.次氯酸中氧原子与氯原子、氢原子之间分别形成1对共用电子对;
B.原子符号左上角为质量数左下角为质子数,质量数=中子数+质子数;
C.氯离子为阴离子,电子式中需要标出最外层的8个电子;
D.质量数=中子数+质子数,原子符号左上角为质量数左下角为质子数.
解答 解:A.次氯酸中氧原子与氯原子、氢原子之间分别形成1对共用电子对,结构式为H-O-Cl,故A错误;
B.质量数为37的氯原子:3717Cl,故B错误;
C.氯化铵为离子化合物,铵根离子和氯离子都需要标出所带电荷和原子的最外层电子,氯化铵正确的电子式为: ,故C错误;
,故C错误;
D.原子核内有10个中子的氧原子,质子数为8,质量数=8+10=18,原子符号188O,故D正确;
故选D.
点评 本题考查了电子式、原子符号、结构式、元素符号等化学用语的判断,题目难度中等,注意掌握常见化学用语的表示方法,明确离子化合物与共价化合物的电子式的区别,试题有利于培养学生灵活应用所学知识的能力.


科目:高中化学 来源: 题型:选择题
| A. | 2.0g H218O与D2O的混合物中所含中子数为NA | |
| B. | 常温常压下,30g丙醇中存在的共价键总数为5NA | |
| C. | 2 mol Cu和足量热浓硫酸反应可生成2NA个SO3分子 | |
| D. | 电解法精炼铜时,若转移的电子数为NA个,则阳极质量减小32g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④⑦⑩ | B. | ①③⑥⑧ | C. | ①④⑧⑨ | D. | ②⑤⑦⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
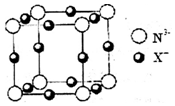 氮是重要的非金属元素,可以形成多种化合物.回答以下问题:
氮是重要的非金属元素,可以形成多种化合物.回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(OCN)64-等.
过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(OCN)64-等. Mg2FeH6+Mg.
Mg2FeH6+Mg.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制一定物质的量浓度的溶液,定容时仰视刻度,溶液浓度偏小 | |
| B. | 酸碱中和滴定时,若未用待测液润洗锥形瓶,对测定结果无影响 | |
| C. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗上口倒出 | |
| D. | 将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤洗涤并收集沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 次氯酸分子的结构式:H-Cl-O | B. | 硫离子的结构示意  | ||
| C. | 质量数为37的氯原子为:37Cl | D. | 二氧化硅的分子式为:SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 60g二氧化硅中含有SiO2分子的数目为NA | |
| B. | 标准状况下,5.6 LCO2与足量Na2O2反应转移的电子数为0.5NA | |
| C. | Zn与足量的浓硫酸反应生成标况下22.4L气体时,转移2NA电子 | |
| D. | 1L 0.1mol/L的Na2CO3溶液中含有的阴离子总数小于0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com