
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:填空题
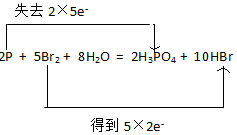 .反应中氧化剂与还原剂的物质的量之比为5:2.
.反应中氧化剂与还原剂的物质的量之比为5:2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2 SO4 | B. | CuSO4 | C. | Na2 SO4 | D. | NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用量筒量取12.12mL的盐酸 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 | |
| C. | 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 称量时,称量物应放在托盘天平的左盘,砝码放在托盘天平的右盘中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将铜插入硝酸银溶液中:Cu+Ag+═Cu2++Ag | |
| B. | Ca( HCO3)2 溶液与过量 NaOH 溶液反应:HCO3-+OH-+Ca2+═CaCO3↓+H2O | |
| C. | 用食醋除水垢:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O | |
| D. | 稀硫酸和Ba(OH)2溶液反应:H++SO42-+Ba 2++OH-═BaSO 4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H1-△H2 | B. | △H2-△H1 | C. | △H1+△H2 | D. | 2△H1-2△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
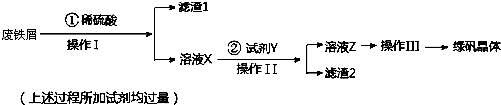
| 氢氧化钠质量(g) | 氯化钠质量(g) | |
| ① | 2.40 | 3.51 |
| ② | 2.32 | 2.34 |
| ③ | 3.48 | 3.51 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1﹕2﹕3 | B. | 1﹕1﹕1 | C. | 2﹕3﹕6 | D. | 3﹕2﹕1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com