
 2CO2+N2���䲿�ֻ�ѧƽ�ⳣ�����±���
2CO2+N2���䲿�ֻ�ѧƽ�ⳣ�����±���| T���棩 | 0 | 50 | 100 |
| K | 0.5 | 1.05 | 2.56 |
 CO2+1/2N2����100��ʱ��K��ֵ= ��
CO2+1/2N2����100��ʱ��K��ֵ= ��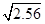 =1.6
=1.6

 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CO��g����3H2��g������H����206 kJ/mol��һ�������������Ϊ1 L���ܱ������г���1 mol CH4��1 mol H2O�����CH4��g����CO��g����Ũ����ʱ��仯������ͼ��ʾ������˵����ȷ���� �� ��
CO��g����3H2��g������H����206 kJ/mol��һ�������������Ϊ1 L���ܱ������г���1 mol CH4��1 mol H2O�����CH4��g����CO��g����Ũ����ʱ��仯������ͼ��ʾ������˵����ȷ���� �� ��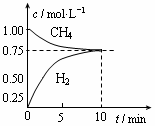
| A��10minʱ��CH4��ʾ�ķ�Ӧ����Ϊ0.075 mol?L��1?min��1 |
| B��ʹ�ø�Ч�����ܹ�����CO�IJ��� |
| C���������·�Ӧ��ƽ�ⳣ��Ϊ0.1875 |
D�������¶���ʹ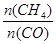 ���� ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3��״̬��ʱ��ƽ�⣬��O2��ת����Ϊ�� ��
2SO3��״̬��ʱ��ƽ�⣬��O2��ת����Ϊ�� ��
| A��40�� | B��60�� | C��80�� | D��90�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ʳ���ڳ����¸������Է����е� | B�����Ƿ��ȷ�Ӧ�����Է��� |
| C���Է���Ӧ����������ķ�Ӧ | D�����صķ�Ӧ�������Է���Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����

 2NH3(g)��CO2(g)��ʵ���ò�ͬ�¶��µ�ƽ�����������±���
2NH3(g)��CO2(g)��ʵ���ò�ͬ�¶��µ�ƽ�����������±���| �¶�(��) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| ƽ����ѹǿ(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| ƽ��������Ũ�� (��10��3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
 NH4HCO3��NH3��H2O�����о�С��ֱ������ݲ�ͬ��ʼŨ�ȵİ����������Һ�ⶨˮ�ⷴӦ���ʣ��õ�c(NH2COO��)��ʱ��仯������ͼ��ʾ��
NH4HCO3��NH3��H2O�����о�С��ֱ������ݲ�ͬ��ʼŨ�ȵİ����������Һ�ⶨˮ�ⷴӦ���ʣ��õ�c(NH2COO��)��ʱ��仯������ͼ��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2AB(g)�ﵽ��ѧƽ��ı�־��
2AB(g)�ﵽ��ѧƽ��ı�־���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����2 sʱ����ϵ��ѹǿΪ��Ӧǰ��1.1���� |
| B��ǰ2 s����N2O4Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ0.01 mol��L-1��s-1 |
| C��ƽ��ʱ����ϵ�ں�N2O4 0.25 mol |
| D��ƽ��ʱ�����������ڳ��뵪����������N2O4��ת���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com