
| A. | 含大量OH-的溶液:Ba2+、K+、NO3-、AlO2- | |
| B. | 加人Na2O2粉末的溶液:Na+、Cl-、SO32-、OH- | |
| C. | c(KNO3)=1.0mol/L的溶液:H+、I-、Cl-、Ca2+ | |
| D. | 滴入紫色石蕊试液呈蓝色的溶液:Fe3+、Ba2+、HCO3-、Br- |
分析 A.离子之间不发生任何反应;
B.Na2O2具有强氧化性;
C.酸性条件下NO3-具有强氧化性;
D.滴入紫色石蕊试液呈蓝色的溶液呈碱性.
解答 解:A.含大量OH-的溶液,Ba2+、K+、NO3-、AlO2-离子之间不发生任何反应,可大量共存,故A正确;
B.Na2O2具有强氧化性,具有还原性的SO32-不能大量存在,故B错误;
C.酸性条件下NO3-具有强氧化性,I-不能大量共存,故C错误;
D.滴入紫色石蕊试液呈蓝色的溶液呈碱性,碱性条件下Fe3+、Ba2+、HCO3-不能大量共存,分别生成氢氧化铁、碳酸钡沉淀,故D错误.
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子的反应为解答的关键,侧重氧化还原反应及复分解反应的离子共存考查,综合性较强,题目难度不大.


科目:高中化学 来源: 题型:实验题
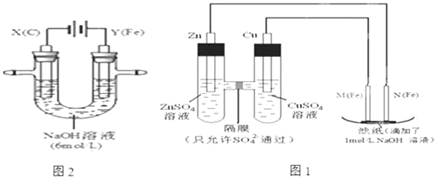
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 无法判断混合物中是否含有Na2O | B. | 由Ⅱ可知X中一定存在SiO2 | ||
| C. | 1.92g固体成分为Cu | D. | 15.6g混合物X中m(Fe2O3):m(Cu)=1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液 | |
| B. | 蒸馏时,温度计的水银球应靠近蒸馏烧瓶的底部 | |
| C. | 容量瓶用水洗净后,可不经干燥直接用于配制溶液 | |
| D. | 配制1L0.1mol/L的NaCl溶液时可用托盘天平称量5.85gNaCl固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2、SiO2的晶体结构类型不同 | |
| B. | 加热硅、硫晶体使之熔化,克服的作用力不同 | |
| C. | HCl、NaCl溶于水,破坏的化学键类型相同 | |
| D. | NaOH、NH4Cl晶体中既有离子键又有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
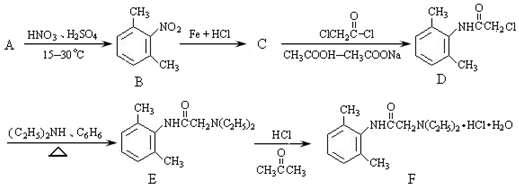
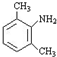 ;
;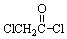 与足量的NaOH溶液共热充分反应的化学方程式:
与足量的NaOH溶液共热充分反应的化学方程式: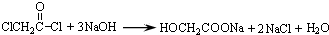 .
.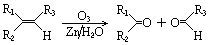
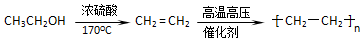
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
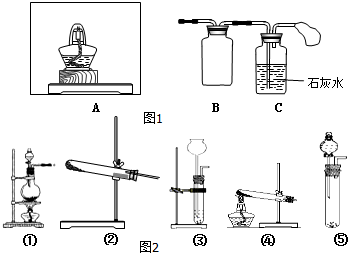 Na2O2是常见的氧化剂,某化学小组的同学欲通过以下实验确定炭粉与Na2O2反应的产物.
Na2O2是常见的氧化剂,某化学小组的同学欲通过以下实验确定炭粉与Na2O2反应的产物.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com