
ŅŃÖŖA£Øg£©+B£Øg£©⇌C£Øg£©+D£Øg£©·“Ó¦µÄĘ½ŗā³£ŹżŗĶĪĀ¶ČµÄ¹ŲĻµČēĻĀ£ŗ
|ĪĀ¶Č/”ę 700 900 830 1000 1200
Ę½ŗā³£Źż 1.7 1.1 1.0 0.6 0.4
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©øĆ·“Ó¦µÄ”÷H 0£ØĢī”°£¼”±”°£¾”±”°=”±£©£»
£Ø2£©830”ꏱ£¬ĻņŅ»øö5LµÄĆܱÕČŻĘ÷ÖŠ³äČė0.20molµÄAŗĶ0.80molµÄB£¬Čō·“Ó¦¾Ņ»¶ĪŹ±¼äŗ󣬓ļµ½Ę½ŗāŹ±AµÄ×Ŗ»ÆĀŹĪŖ80%£¬Čē¹ūÕāŹ±ĻņøĆĆܱÕČŻĘ÷ÖŠŌŁ³äČė1molė²Ęų£¬Ę½ŗāŹ±AµÄ×Ŗ»ÆĀŹ»į £ØĢī”°±ä“ó”±”¢”°±äŠ””±»ņ”°²»±ä”±£©
£Ø3£©Čō±£³ÖČŻĘ÷µÄČŻ»ż²»±ä£¬ŌņøĆ·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŅĄ¾ŻŹĒ £ØĢīŠņŗÅ£©£®
a£®µ„Ī»Ź±¼äĄļÉś³ÉBŗĶDµÄĪļÖŹµÄĮæĻąµČ
b£®ĘųĢåµÄĆÜ¶Č²»Ėꏱ¼äøıä
c£®ČŻĘ÷ÄŚŃ¹Ēæ±£³Ö²»±ä
d£®»ģŗĻĘųĢåµÄĘ½¾łÄ¦¶ūÖŹĮæ±£³Ö²»±ä
£Ø4£©1200”ꏱ·“Ó¦C£Øg£©+D£Øg£©⇌A£Øg£©+B£Øg£©µÄĘ½ŗā³£ŹżµÄ ÖµĪŖ £®
ÖµĪŖ £®
æ¼µć£ŗ »ÆŃ§Ę½ŗāµÄ¼ĘĖć£»»ÆŃ§Ę½ŗāדĢ¬µÄÅŠ¶Ļ£®
·ÖĪö£ŗ £Ø1£©»ÆŃ§Ę½ŗā³£Źż£¬ŹĒÖøŌŚŅ»¶ØĪĀ¶ČĻĀ£¬æÉÄę·“Ó¦“ļµ½Ę½ŗāŹ±ø÷Éś³ÉĪļÅØ¶ČµÄ»Æѧ¼ĘĮæŹż“ĪĆŻµÄ³Ė»ż³żŅŌø÷·“Ó¦ĪļÅØ¶ČµÄ»Æѧ¼ĘĮæŹż“ĪĆŻµÄ³Ė»żĖłµĆµÄ±ČÖµ£¬¾Ż“ĖŹéŠ“£»
ÓɱķÖŠŹż¾ŻæÉÖŖ£¬ĪĀ¶ČŌ½øßĘ½ŗā³£ŹżŌ½Š”£¬ĖµĆ÷ÉżøßĪĀ¶ČĘ½ŗāĻņÄę·“Ó¦ŅĘ¶Æ£¬¹ŹÕż·“Ó¦ŹĒ·ÅČČ·“Ó¦£»
£Ø2£©ÉčĘ½ŗāŹ±AµÄÅØ¶Č±ä»ÆĮæĪŖx£¬ĄūÓĆČż¶ĪŹ½±ķŹ¾Ę½ŗāŹ±ø÷×é·ÖµÄĘ½ŗāÅØ¶Č£¬“śČėĘ½ŗā³£ŹżĮŠ·½³Ģ¼ĘĖćxµÄÖµ£¬ŌŁøł¾Ż×Ŗ»ÆĀŹ¶ØŅå¼ĘĖć£»
Ģå»ż²»±ä£¬³äČė1molė²Ęų£¬·“Ó¦»ģŗĻĪļø÷×é·ÖµÄÅØ¶Č²»±ä£¬±ä»Æ²»ŅĘ¶Æ£¬AµÄ×Ŗ»ÆĀŹ²»±ä£»
£Ø3£©øł¾Ż»ÆŃ§Ę½ŗāדĢ¬µÄĢŲÕ÷½ā“š£¬µ±·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬ø÷ĪļÖŹµÄÅØ¶Č”¢°Ł·Öŗ¬Įæ²»±ä£¬ŅŌ¼°ÓÉ“ĖŃÜÉśµÄŅ»Š©ĮæŅ²²»·¢Éś±ä»Æ£¬½āĢāŹ±ŅŖ×¢Ņā£¬Ń”ŌńÅŠ¶ĻµÄĪļĄķĮ棬Ėę×Å·“Ó¦µÄ½ųŠŠ·¢Éś±ä»Æ£¬µ±øĆĪļĄķĮæÓɱä»Æµ½¶ØÖµŹ±£¬ĖµĆ÷æÉÄę·“Ó¦µ½“ļĘ½ŗāדĢ¬£»
£Ø4£©Ķ¬Ņ»·“Ó¦ŌŚĻąĶ¬ĪĀ¶ČĻĀ£¬Õż”¢Äę·“Ó¦·½ĻņµÄĘ½ŗā³£Źż»„ĪŖµ¹Źż£®
½ā“š£ŗ ½ā£ŗ£Ø1£©ÓɱķÖŠŹż¾ŻæÉÖŖ£¬ĪĀ¶ČŌ½øßĘ½ŗā³£ŹżŌ½Š”£¬ĖµĆ÷ÉżøßĪĀ¶ČĘ½ŗāĻņÄę·“Ó¦ŅĘ¶Æ£¬¹ŹÕż·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬¼“”÷H£¼0£¬¹Ź“š°øĪŖ£ŗ£¼£»
£Ø2£©·“Ó¦³õŹ¼6sÄŚAµÄĘ½¾ł·“Ó¦ĖŁĀŹv£ØA£©=0.003mol•L﹣1•s﹣1£¬Ōņ6sÄŚ”÷c£ØA£©=0.003mol•L﹣1•s﹣1”Į6s=0.018mol/L£¬AµÄĘšŹ¼ÅضČĪŖ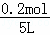 =0.04mol/L£¬¹Ź6sŹ±Ź±c£ØA£©=0.04mol/L﹣0.018mol/L=0.022mol/L£¬¹Ź6sÄŚ”÷n£ØA£©=0.018mol/L”Į5L=0.09mol£¬ÓÉ·½³ĢŹ½æÉÖŖn£ØC£©=”÷n£ØA£©=0.09mol£¬
=0.04mol/L£¬¹Ź6sŹ±Ź±c£ØA£©=0.04mol/L﹣0.018mol/L=0.022mol/L£¬¹Ź6sÄŚ”÷n£ØA£©=0.018mol/L”Į5L=0.09mol£¬ÓÉ·½³ĢŹ½æÉÖŖn£ØC£©=”÷n£ØA£©=0.09mol£¬
ÉčĘ½ŗāŹ±AµÄÅØ¶Č±ä»ÆĮæĪŖx£¬Ōņ£ŗ
A£Øg£©+B£Øg£©⇌C£Øg£©+D£Øg£©
æŖŹ¼£Ømol/L£©£ŗ0.04 0.16 0 0
±ä»Æ£Ømol/L£©£ŗx x x x
Ę½ŗā£Ømol/L£©£ŗ0.04﹣x 0.16﹣x x x
¹Ź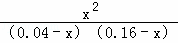 =1£¬½āµĆx=0.032
=1£¬½āµĆx=0.032
ĖłŅŌĘ½ŗāŹ±AµÄ×Ŗ»ÆĀŹĪŖ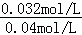 ”Į100%=80%£¬
”Į100%=80%£¬
Ģå»ż²»±ä£¬³äČė1molė²Ęų£¬·“Ó¦»ģŗĻĪļø÷×é·ÖµÄÅØ¶Č²»±ä£¬±ä»Æ²»ŅĘ¶Æ£¬AµÄ×Ŗ»ÆĀŹ²»±ä£¬
¹Ź“š°øĪŖ£ŗ80%£»²»±ä£»
£Ø3£©a£®µ„Ī»Ź±¼äĄļÉś³ÉBŗĶDµÄĪļÖŹµÄĮæĻąµČ£¬ĖµĆ÷µ„Ī»Ź±¼äÄŚÉś³ÉµÄĪļÖŹµÄĮæÓėĻūŗÄBµÄĪļÖŹµÄĮæĻąµČ£¬ĖµĆ÷µ½“ļĘ½ŗā£¬¹ŹaÕżČ·£»
b£®»ģŗĻĘųĢåµÄ×ÜÖŹĮæ²»±ä£¬ČŻĘ÷µÄČŻ»ż²»±ä£¬¹Ź»ģŗĻĘųĢåµÄĆܶȏ¼ÖÕ²»±ä£¬¹ŹĘųĢåµÄĆÜ¶Č²»Ėꏱ¼äøı䣬²»ÄÜĖµĆ÷µ½“ļĘ½ŗā£¬¹Źb“ķĪó£¬
c£®øĆ·“Ó¦Ē°ŗóĘųĢåµÄĪļÖŹµÄĮæ²»±ä£¬Ń¹ĒæŹ¼ÖÕ²»±ä£¬¹ŹŃ¹Ēæ²»Ėꏱ¼äøı䣬²»ÄÜĖµĆ÷µ½“ļĘ½ŗā£¬¹Źc“ķĪó£¬
d£®»ģŗĻĘųĢåµÄ×ÜÖŹĮæ²»±ä£¬ČŻĘ÷µÄČŻ»ż²»±ä£¬ĪļÖŹµÄĮæ²»±ä£¬»ģŗĻĘųĢåµÄĘ½¾łÄ¦¶ūÖŹĮæ±£³Ö²»±ä£¬²»ÄÜĖµĆ÷µ½“ļĘ½ŗā£¬¹Źd“ķĪó£¬
¹Ź“š°øĪŖ£ŗa£»
£Ø4£©Ķ¬Ņ»·“Ó¦ŌŚĻąĶ¬ĪĀ¶ČĻĀ£¬Õż”¢Äę·“Ó¦·½ĻņµÄĘ½ŗā³£Źż»„ĪŖµ¹Źż£¬¹Ź1200”ꏱ·“Ó¦C£Øg£©+D£Øg£©⇌A£Øg£©+B£Øg£©µÄĘ½ŗā³£ŹżµÄÖµĪŖ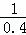 =2.5£¬
=2.5£¬
¹Ź“š°øĪŖ£ŗ2.5£®
µćĘĄ£ŗ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗā¼ĘĖć”¢Ę½ŗā³£Źż¼ĘĖć”¢»Æѧ·“Ó¦ĖŁĀŹ”¢Ę½ŗāדĢ¬ÅŠ¶Ļ£¬ÄѶČÖŠµČ£¬×¢Ņā»ÆŃ§Ę½ŗāדĢ¬ÅŠ¶Ļ£¬Ń”ŌńÅŠ¶ĻµÄĪļĄķĮ棬Ėę×Å·“Ó¦µÄ½ųŠŠ·¢Éś±ä»Æ£¬µ±øĆĪļĄķĮæÓɱä»Æµ½¶ØÖµŹ±£¬ĖµĆ÷æÉÄę·“Ó¦µ½“ļĘ½ŗāדĢ¬£®


 ø÷µŲĘŚÄ©ø“Ļ°ĢŲѵ¾ķĻµĮŠ“š°ø
ø÷µŲĘŚÄ©ø“Ļ°ĢŲѵ¾ķĻµĮŠ“š°ø Š”²©ŹæĘŚÄ©“³¹Ų100·ÖĻµĮŠ“š°ø
Š”²©ŹæĘŚÄ©“³¹Ų100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠŅĄ¾ŻČČ»Æѧ·½³ĢŹ½µĆ³öµÄ½įĀŪÕżČ·µÄŹĒ£Ø£©
A£® ŅŃÖŖ2H2£Øg£©+O2£Øg£©=2H2O£Øg£©”÷H=﹣483.6 kJ•mol﹣1£¬ŌņĒāĘųµÄČ¼ÉÕČČĪŖ241.8 kJ•mol﹣1
B£® ŅŃÖŖNaOH£Øaq£©+HCl£Øaq£©=NaCl£Øaq£©+H2O£Øl£©”÷H=﹣57.3 kJ•mol﹣1£¬Ōņŗ¬40.0g NaOHµÄĻ”ČÜŅŗÓėĻ”“×ĖįĶźČ«ÖŠŗĶ£¬·Å³öŠ”ÓŚ57.3kJµÄČČĮæ
C£® ¼ŗÖŖ2C£Øs£©+2O2£Øg£©=2CO2£Øg £©”÷H=a£»2C£Øs£©+O2£Øg£©=2CO£Øg£©£»”÷H=b£¬Ōņa£¾b
£©”÷H=a£»2C£Øs£©+O2£Øg£©=2CO£Øg£©£»”÷H=b£¬Ōņa£¾b
D£® ŅŃÖŖC£ØŹÆÄ«£¬s£©=C£Ø½šøÕŹÆ£¬s£©”÷H£¾0£¬ŌņŹÆÄ«±Č½šøÕŹÆĪȶØ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
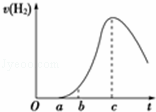
½«ŌŚæÕĘųÖŠ¾ĆÖƵÄĀĮʬÓė0.5mol•L﹣1ĮņĖį·“Ó¦£¬²śÉśĒāĘųµÄĖŁĀŹÓė·“Ó¦Ź±¼äæÉÓĆČēĶ¼ĖłŹ¾µÄĒśĻß±ķŹ¾£¬ŹŌ»Ų“šĻĀĮŠĪŹĢā£®
£Ø1£©ĒśĻßO”śa¶Ī²»²śÉśĒāĘųµÄÖ÷ŅŖŌŅņŹĒ£ØÓĆÓŠ¹Ų»Æѧ·½³ĢŹ½±ķŹ¾£©£ŗ £®
£Ø2£©ĒśĻßb”śc¶Ī²śÉśĒāĘųµÄĖŁĀŹŌö¼Ó½ĻæģµÄÖ÷ŅŖŌŅņŹĒ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ČēĶ¼ĖłŹ¾£¬”÷H1=﹣393.5kJ•mol﹣1£¬”÷H2=﹣395.4kJ•mol﹣1£¬ĻĀĮŠĖµ·Ø»ņ±ķŹ¾Ź½ÕżČ·µÄŹĒ£Ø£©
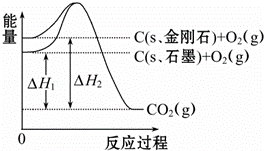
A£® C£Øs”¢ŹÆÄ«£©═C£Øs”¢½šøÕŹÆ£©”÷H=+1.9 kJ•mol﹣1
B£® ŹÆÄ«ŗĶ½šøÕŹÆµÄ×Ŗ»ÆŹĒĪļĄķ±ä»Æ
C£® ½šøÕŹÆµÄĪČ¶ØŠŌĒæÓŚŹÆÄ«
D£® 1 molŹÆÄ«µÄÄÜĮæ±Č1 mol½šøÕŹÆµÄ×ÜÄÜĮæ“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ČēĶ¼ĖłŹ¾£¬Ķʬ”¢ŠæʬŗĶŹÆÄ«°ōÓƵ¼ĻßĮ¬½Óŗó²åČė·¬ĒŃĄļ£¬µēĮ÷¼ĘÖŠÓŠµēĮ÷Ķعż£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø£©
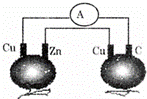
A£® ŠæʬŹĒøŗ¼« B£® Į½øöĶʬÉĻ¶¼·¢ÉśŃõ»Æ·“Ó¦
C£® ŹÆÄ«ŹĒŅõ¼« D£® Į½øö·¬ĒѶ¼ŠĪ³ÉŌµē³Ų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¹ŲÓŚČČ»Æѧ·½³ĢŹ½£ŗ2H2£Øg£©+02£Øg£©=2H20£Ø1£©£¬”÷H=﹣571.6kJ•mol﹣1£¬ĻĀĮŠÓŠ¹ŲŠšŹö²»ÕżČ·µÄŹĒ£Ø£©
A£® 2mol H2ĶźČ«Č¼ÉÕÉś³ÉŅŗĢ¬Ė®Ź±·Å³ö571.6 kJµÄČČ
B£® 1mol H2ĶźČ«Č¼ÉÕÉś³ÉŅŗĢ¬Ė®Ź±·Å³ö285.8kJµÄČČ
C£® 2øöĒā·Ö×ÓĶźČ«Č¼ÉÕÉś³ÉŅŗĢ¬Ė®Ź±·Å³ö571.6 kJµÄČČ
D£® ÉĻŹöČČ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖH2£Øg£©+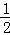 O2£Øg£©=H20£Ø1£©£¬”÷H=﹣285.8 kJ•mol﹣1
O2£Øg£©=H20£Ø1£©£¬”÷H=﹣285.8 kJ•mol﹣1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijĆܱÕČŻĘ÷ÖŠ·¢ÉśČēĻĀ·“Ó¦£ŗX£Øg£©+3Y£Øg£©2Z£Øg£©”÷H£¼0£®ĻĀĶ¼±ķŹ¾øĆ·“Ó¦µÄĖŁĀŹ£Ø¦Ō£©Ėꏱ¼ä£Øt£©±ä»ÆµÄ¹ŲĻµ£¬t2”¢t3”¢t5Ź±æĢĶā½ēĢõ¼žÓŠĖłøı䣬µ«¶¼Ć»ÓŠøıäø÷ĪļÖŹµÄ³õŹ¼¼ÓČėĮ森ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø£©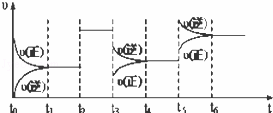
A£® t3Ź±½µµĶĮĖĪĀ¶Č
B£® t5Ź±Ōö“óĮĖŃ¹Ēæ
C£® t2Ź±¼ÓČėĮĖ“߻ƼĮ
D£® t4”«t5Ź±¼äÄŚ×Ŗ»ÆĀŹŅ»¶Ø×īµĶ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ»Æѧ·½³ĢŹ½“ķĪóµÄŹĒ (””””)”£
A£®Ca(HCO3)2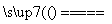 CaCO3”ż£«CO2”ü£«H2O
CaCO3”ż£«CO2”ü£«H2O
B£®Mg(HCO3)2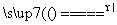 MgCO3”ż£«CO2”ü£«H2O
MgCO3”ż£«CO2”ü£«H2O
C£®MgCO3£«H2O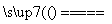 Mg(OH)2”ż£«CO2”ü
Mg(OH)2”ż£«CO2”ü
D£®CaCO3£«H2O===Ca(OH)2£«CO2”ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠø÷×éĄė×ÓÄܹ»“óĮæ¹²“ęµÄŹĒ£Ø£©
A£® pH=0µÄČÜŅŗÖŠ£ŗFe3+”¢Mg2+”¢Cl﹣”¢SO42﹣
B£® ÄÜÓėĀĮ·“Ӧɜ³ÉĒāĘųµÄČÜŅŗÖŠ£ŗK+”¢HC03﹣”¢Cl﹣”¢S2﹣
C£® Ź¹pHŹŌÖ½ĻŌĄ¶É«µÄČÜŅŗÖŠ£ŗCu2+”¢Fe3+”¢N03﹣”¢SO42﹣
D£® ŌŚA1C13ČÜŅŗÖŠ£ŗNa+”¢﹣”¢SO42﹣”¢N03﹣
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com