
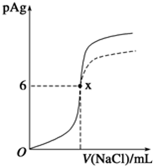
 已知:pAg=-lg{c(Ag+)},Ksp(AgCl)=1×10-12.如图是向10mL AgNO3溶液中逐渐加入0.1mol?L-1的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).根据图象所得下列结论正确的是[提示:Ksp(AgCl)>Ksp(AgI)]( )
已知:pAg=-lg{c(Ag+)},Ksp(AgCl)=1×10-12.如图是向10mL AgNO3溶液中逐渐加入0.1mol?L-1的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).根据图象所得下列结论正确的是[提示:Ksp(AgCl)>Ksp(AgI)]( )| A、原AgNO3溶液的物质的量浓度为1mol?L-1 |
| B、图中x点的坐标为(100,6) |
| C、若升高温度,图象不会发生变化 |
| D、把0.1mol?L-1的NaCl换成0.1mol?L-1 NaI则图象在终点后变为虚线部分 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、488.3kJ?mol-1 |
| B、-244.15kJ?mol-1 |
| C、244.15kJ?mol-1 |
| D、-488.3kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将一定量氨气通入0.1 mol?L-1 NH4Cl溶液中可能有:c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| B、AgCl沉淀易转化成AgI沉淀且Ksp(AgX)=c(Ag+)?c(X-),故Ksp(AgI)>K(AgCl) |
| C、F、Cl、Br、I的非金属性逐渐减弱,HF、HCl、HBr、HI水溶液的酸性逐渐减弱 |
| D、短周期元素形成离子后,最外层均达8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 靛蓝是一种食品用合成色素,但对人体有害.使用时必须严格控制使用量.靛蓝允许小于0.1g?kg-1.靛蓝结构简式如图所示.下列关于靛蓝的叙述错误的是( )
靛蓝是一种食品用合成色素,但对人体有害.使用时必须严格控制使用量.靛蓝允许小于0.1g?kg-1.靛蓝结构简式如图所示.下列关于靛蓝的叙述错误的是( )| A、靛蓝可与溴水发生加成反应,使溴水褪色 |
| B、它的分子式是C16H10N2O2 |
| C、该物质分子量较大是高分子化合物 |
| D、它与氢气发生加成反应,1mol靛蓝需氢气最大量是9mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、40 mL 0.03 mol?L-1HCl溶液 |
| B、20 mL 0.02 mol?L-1KCl溶液 |
| C、30 mL 0.02 mol?L-1CaCl2溶液 |
| D、50 mL 0.05 mol?L-1AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加过量KI溶液充分反应后,Ksp(AgCl)减小 |
| B、加过量KI溶液充分反应后,溶液中Ag+和I-的浓度之积等于Ksp(AgI) |
| C、加过量KI溶液充分反应后,溶液中Ag+和Cl-的浓度之积小于Ksp(AgCl) |
| D、Ksp(AgI)<Ksp(AgCl) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验操作 | 现象 | 结论 | |
| A | 向盛有25mL沸水的烧杯中滴加5~6滴FeCl3饱和溶液,继续煮沸 | 溶液生成红褐色沉淀 | 制得Fe(OH)3胶体 |
| B | 向两支盛有KI3溶液的试管中,分别滴加淀粉溶液和AgNO3溶液, | 前者溶液变蓝, 后者有黄色沉淀 | KI3溶液中存在平衡: I3-?I2+I- |
| C | 将溴乙烷和NaOH乙醇溶液混合加热,产生气体通入酸性KMnO4溶液 | 酸性KMnO4溶液 褪色 | 产生了乙烯 |
| D | 蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再加入新制银氨溶液,水浴加热 | 出现红色沉淀 | 蔗糖水解已水解 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com