
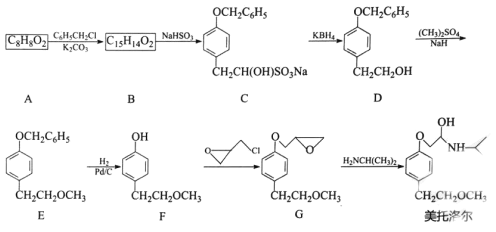
【题目】美托洛尔可治疗各型高血压及作血管扩张剂,它的一种合成路线如下:
已知:![]() +
+![]()
![]()
![]() +HCl
+HCl
(1)A的化学名称是 _________,B的结构简式为__________,美托洛尔中含氧官能团的名称是_____________。
(2)A合成B的反应中,加人K2CO3的作用可能是 _________。
(3)B合成C的反应类型是________ 。
(4)F生成G的化学方程式为________ 。
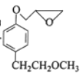
(5)氯甲基环氧乙烷(![]() ) 是合成有机化合物的重要原料,实验室检验卤代烃中氯原子的常用试剂是______。
) 是合成有机化合物的重要原料,实验室检验卤代烃中氯原子的常用试剂是______。
(6)芳香族化合物M是F的同分异构体.则符合下列条件的M共有___种(不含立体异构)。
①苯环上只有2个取代基
②1molM与足量 Na 充分反应能生成1mol H2
③能与FeCl3溶液发生显色反应。
其中核磁共振氢谱为5组峰同分异构体的结构简式为_______。
【答案】对羟基苯乙醛 ![]() 醚键、羟基 消耗反应生成的HCl,有利于反应正向进行,有利于提高的B的产率 加成反应
醚键、羟基 消耗反应生成的HCl,有利于反应正向进行,有利于提高的B的产率 加成反应 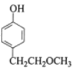 +
+![]()
![]()
 +HCl NaOH水溶液、硝酸、硝酸银溶液 15
+HCl NaOH水溶液、硝酸、硝酸银溶液 15 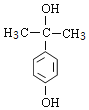
【解析】
A的分子式为C8H8O2,不饱和度为5,说明除苯环外还有一个双键,A发生信息中取代反应生成B,B与A相比多了7个碳原子,说明A中只有一个酚羟基,且该过程中A的双键没有打开;B与亚硫酸氢钠发生反应生成C,根据C的结构简式可知,B到C的过程中双键打开,所以该过程应为加成反应,且根据C的结构简式可反推出中A和B中的双键应为醛基,所以A为![]() 、B为
、B为![]() 。
。
(1)根据分析可知A为![]() ,名称为对羟基苯乙醛;B的结构简式为
,名称为对羟基苯乙醛;B的结构简式为![]() ;由结构可知美托洛尔中含氧官能团为:醚键、羟基;
;由结构可知美托洛尔中含氧官能团为:醚键、羟基;
(2)A发生取代反应有HCl生成,加入K2CO3的作用可能是:消耗反应生成的HCl,有利于反应正向进行,有利于提高的B的产率;
(3)根据分析可知B到C的反应为加成反应;
(4)对比F、G的结构,可知F中羟基上H原子被![]() 替代生成G,同时生成HCl,反应方程式为:
替代生成G,同时生成HCl,反应方程式为: +
+![]()
![]()
 +HCl;
+HCl;
(5)先进行水解或消去反应使氯元素以氯离子形成进入溶液,再用硝酸酸化,最后用硝酸银溶液检验氯离子,故实验室检验氯原子所用的试剂是:NaOH水溶液、硝酸、硝酸银溶液;
(6)芳香族化合物M是F的同分异构体,且符合下列条件:③能与FeCl3溶液发生显色反应,说明含有酚羟基,②1mol M与足量Na充分反应能生成1mol H2,说明分子中有2个-OH,①苯环上只有2个取代基,其中1个为-OH,另一个为CH3CH2CH2OH或![]() 中烃基去掉1个H原子形成的基团,前者有3种、后者有2种,与酚羟基均有邻、间、对3种位置结构,故符合条件的共有:3×(3+2)=15种,其中核磁共振氢谱为5组峰同分异构体的结构简式为:
中烃基去掉1个H原子形成的基团,前者有3种、后者有2种,与酚羟基均有邻、间、对3种位置结构,故符合条件的共有:3×(3+2)=15种,其中核磁共振氢谱为5组峰同分异构体的结构简式为: 。
。


科目:高中化学 来源: 题型:
【题目】一种由甲苯合成多取代芳香族化合物的反应路线如图:
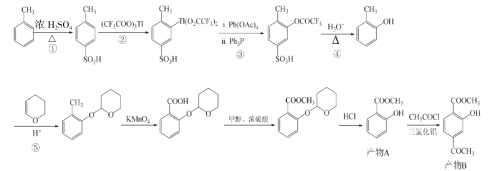
回答下列问题:
(1)甲苯分子中最多有 __________个原子共平面
(2)写出反应②的化学方程式___________ ,反应类型为 _______。
(3)甲苯易在甲基的邻、对位发生反应,若不进行反应①,直接进行反应②~④,可能会得到的副产物的结构简式有 ________________(写出两种)。
(4)反应⑤的目的是_____________________。
(5)产物A与足量氢气加成后的产物,核磁共振氢谱有_____个峰,1mol 产物B可与___mol氢氧化钠溶液反应。
(6)不改变取代基的结构与个数,产物B的同分异构体(不包括B)有______种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚铁氰化钾(K4[Fe(CN)6])双称黄血盐,是一种重要的化工原料。检验三价铁发生的反应为:K4[Fe(CN)6]+FeCl3=KFe[Fe(CN)6]↓(滕氏蓝) +3KCl,回答问题:
(1)写出基态Fe3+的核外电子排布式_________。
(2)K4[Fe(CN)6]中的作用力除共价键外,还有______和________。含有12mol σ键的K4[Fe(CN)6的物质的量为________mol。
(3)黄血盐中N原子的杂化方式为______;C、N、O的第一电离能由大到小的排序为_____,电负性由大到小的排序为________。
(4)Fe、Na、K的晶体结构如图所示:
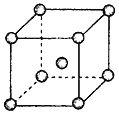
① 钠的熔点比钾更高,原因是__________________________。
② Fe原子半径是r cm,阿伏加德罗常数为NA,铁的相对原子质量为a,则铁单质的密度是_______g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃的结构简式为![]() ,关于该有机物,下列叙述正确的是( )
,关于该有机物,下列叙述正确的是( )
A. 所有碳原子可能处于同一平面
B. 属于芳香族化合物的同分异构体有三种
C. 能发生取代反应、氧化反应和加成反应
D. 能使溴水、酸性KMnO4溶液褪色且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中符合下列图像的是( )

A. N2(g)+3H2(g)![]() 2NH3(g) ΔH=-Q1kJ·mol-1(Q1>0)
2NH3(g) ΔH=-Q1kJ·mol-1(Q1>0)
B. 2SO3(g)![]() 2SO2(g)+O2(g) ΔH=+Q2kJ·mol-1(Q2>0)
2SO2(g)+O2(g) ΔH=+Q2kJ·mol-1(Q2>0)
C. 4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH=-Q3kJ·mol-1(Q3>0)
4NO(g)+6H2O(g) ΔH=-Q3kJ·mol-1(Q3>0)
D. H2(g)+CO(g)![]() C(s)+H2O(g) ΔH=+Q4kJ·mol-1(Q4>0)
C(s)+H2O(g) ΔH=+Q4kJ·mol-1(Q4>0)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一容积可变的密闭容器中加入WO3和H2进行反应:WO3(s)+3H2(g)![]() W(s)+3H2O(g),下列说法不正确的是( )
W(s)+3H2O(g),下列说法不正确的是( )
A.将容器的体积缩小一半,其反应速率增大
B.保持体积不变,充入氩气,其反应速率不变
C.保持压强不变,充入氖气,H2O(g)的生成速率增大
D.保持压强不变,充入氖气,H2O(g)、H2(g)的生成速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是( )

A.a电极是负极
B.b电极的电极反应为:4OH--4e-====2H2O+O2↑
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二次电池充放电时总反应可表示为Fe+Ni2O3+3H2O![]() Fe(OH)2+2Ni(OH)2,下列说法正确的是( )
Fe(OH)2+2Ni(OH)2,下列说法正确的是( )
A.该电池可用H2SO4溶液作电解液
B.放电时,当有1molFe(OH)2生成时,电解质溶液中通过的电子数为2NA
C.放电时,Fe所在的电极发生还原反应
D.充电时,阳极的电极反应式为2Ni(OH)2+2OH--2e-=Ni2O3+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】家用炒菜铁锅用水清洗放置后会出现红棕色的锈斑,某同学欲对其原理及条件进行分析。该同学准备了下列实验用品:20%的NaCl溶液、蒸馏水、酚酞试液、KSCN溶液、新制氯水、纯铁丝、碳棒、U形管、导线等;请设计一个实验方案验证铁被腐蚀的电极产物,简述操作过程并写出溶液中有关反应的离子方程式:________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com