
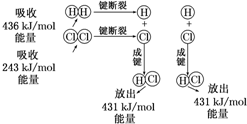
 在25℃、101kPa的条件下,断裂1mol H-H键吸收436kJ能量,断裂1mol Cl-Cl键吸收243kJ能量,形成1mol H-Cl键放出431kJ能量.
在25℃、101kPa的条件下,断裂1mol H-H键吸收436kJ能量,断裂1mol Cl-Cl键吸收243kJ能量,形成1mol H-Cl键放出431kJ能量. .
. 分析 (1)反应物断键吸收的总能量为氢气和氯气的键能和;生成物成键放出的总能量为2molHCl的总键能;根据生成物的键能与反应物的键能的大小关系分析;
(2)化学中常在元素符号周围用小黑点“•”或小叉“×”来表示元素原子的最外层电子,相应的式子叫做电子式,用电子式表示化合物形成过程时,应先判定化合物类型,若为离子化合物,则用箭头表示电子的移动,若为共价化合物,则不需要箭头表示.
解答 解:(1)反应物断键吸收的总能量为氢气和氯气的键能和,则反应物断键吸收的总能量为436+243=679KJ,生成物成键放出的总能量为2molHCl的总键能,则生成物成键放出的总能量为431×2=862KJ,反应热=生成物的键能减反应物的键能=436kJ•mol-1+243kJ•mol-1-2×431 kJ•mol-1=-183kJ•mol-1,△H<0,所以该反应为放热反应,故答案为:679KJ;862KJ;放出;
(2)HCl属于共价化合物,氢原子最外层电子与Cl最外层电子形成一对共用电子对,其形成过程可写为: ,
,
故答案为: ;
;
点评 本题主要考查了化学反应与能量的变化、电子式书写,注意根据键能判断△H,题目难度不大,注意知识的积累.


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 物质 | 除杂试剂 | 分离方法 |
| A | 乙醇 (乙酸) | NaOH溶液 | 蒸馏 |
| B | 甲烷(乙烯) | 酸性KMnO4溶液 | 洗气 |
| C | 苯(苯酚) | 浓溴水 | 过滤 |
| D | 溴乙烷(溴) | NaOH溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HgCl2 属于共价化合物 | B. | HgCl2 属于离子化合物 | ||
| C. | HgCl2 属于非电解质 | D. | HgCl2属于强电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaBr2 | B. | CaCl2 | C. | MgCl2 | D. | MgF2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
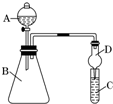 某同学利用如图装置来验证同主族元素非金属性的变化规律.
某同学利用如图装置来验证同主族元素非金属性的变化规律.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 NPG(新戊二醇)是一种可用作太阳能储存热量的物质.已知:NPG的结构式如图.有关NPG的说法不正确的是( )
NPG(新戊二醇)是一种可用作太阳能储存热量的物质.已知:NPG的结构式如图.有关NPG的说法不正确的是( )| A. | NPG的分子式为C5H12O2 | B. | NPG沸点比乙二醇的高 | ||
| C. | NPG一定条件下能发生消去反应 | D. | NPG的氧化产物可发生银镜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 负极反应式:O2+2H2O+4e-═4OH- | |
| B. | 负极反应式:CH4+8OH--8e-═CO2+6H2O | |
| C. | 随着放电的进行,溶液中的氢氧根离子浓度不变 | |
| D. | 放电时溶液中的阴离子向负极移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com