
已知:2H2(g)+O2(g)===2H2O(l)
ΔH=-571.6 kJ·mol-1
2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l)
ΔH=-1 452 kJ·mol-1
H+(aq)+OH-(aq)===H2O(l)
ΔH=-57.3 kJ·mol-1
下列说法正确的是
A.H2(g)的燃烧热为571.6 kJ·mol-1
B. H2SO4(aq)+
H2SO4(aq)+ Ba(OH)2(aq)===
Ba(OH)2(aq)=== BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
C.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多
D.3H2(g)+CO2(g)===CH3OH(l)+H2O(l)
ΔH=+135.9 kJ·mol-1
解析 燃烧热是指在25 ℃、101 kPa下,1 mol纯物质完全燃烧生成稳定氧化物时所放出的热量。A项中根据已知热化学方程式可知H2(g)的燃烧热为285.8 kJ·mol-1,不正确;B项中有BaSO4(s)生成,而生成BaSO4也是放热的,所以放出的热量比57.3 kJ多,即B项中的ΔH<-57.3 kJ·mol-1,不正确;C项,1 g H2(g)完全燃烧放出的热量为 =142.9 kJ,1 g CH3OH(g)完全燃烧放出的热量
=142.9 kJ,1 g CH3OH(g)完全燃烧放出的热量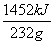 =22.7 kJ,所以同质量时,H2(g)放出热量多,正确;D项中由盖斯定律可知正确的热化学方程式是3H2(g)+CO2(g)===CH3OH(l)+H2O(l) ΔH=-131.4 kJ·mol-1。
=22.7 kJ,所以同质量时,H2(g)放出热量多,正确;D项中由盖斯定律可知正确的热化学方程式是3H2(g)+CO2(g)===CH3OH(l)+H2O(l) ΔH=-131.4 kJ·mol-1。
答案 C


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。
请回答下列问题:
(1)Y在元素周期表中的位置为 。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是 (写化学式),非金属气态氢化物还原性最强的是 (写化学式)。
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有______________
(写出其中两种物质的化学式)。
(4)ZX的电子式为 。[
查看答案和解析>>
科目:高中化学 来源: 题型:
氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如图所示:

请回答下列问题:
(1)由B2O3制备BF3、BN的化学方程式依次是__________________________________、
___________________________________________________________________________;
(2)基态B___________________________________________________________________;
B和N相比,电负性较大的是________,BN中B元素的化合价为________;
(3)在BF3分子中,F—B—F的键角是________,B原子的杂化轨道类型为________,BF3和过量NaF作用可生成NaBF4,BF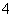 的立体构型为____________;
的立体构型为____________;
(4)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间化学键为____________,层间作用力为___________________________________________________________________;
(5)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5 pm。立方氮化硼晶胞中含有________个氮原子、________个硼原子,立方氮化硼的密度是________ g·cm-3(只要求列算式,不必计算出数值。阿伏加德罗常数为NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.NaHCO3+H2 HCOONa+H2O反应中,储氢、释氢过程均无能量变化
HCOONa+H2O反应中,储氢、释氢过程均无能量变化
B.如图表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化

C.化学反应有新物质生成,并遵循质量守恒定律和能量守恒定律
D.2SO2(g)+O2(g)===2SO3(g)和4SO2(g)+2O2(g)===4SO3(g)的ΔH相等
查看答案和解析>>
科目:高中化学 来源: 题型:
在1 200 ℃时,天然气脱硫工艺中会发生下列反应
H2S(g)+ O2(g)===SO2(g)+H2O(g) ΔH1
O2(g)===SO2(g)+H2O(g) ΔH1
2H2S(g)+SO2(g)=== S2(g)+2H2O(g) ΔH2
S2(g)+2H2O(g) ΔH2
H2S(g)+ O2(g)===S(g)+H2O(g) ΔH3
O2(g)===S(g)+H2O(g) ΔH3
2S(g)===S2(g) ΔH4
则ΔH4的正确表达式为
A.ΔH4= (ΔH1+ΔH2-3ΔH3)
(ΔH1+ΔH2-3ΔH3)
B.ΔH4= (3ΔH3-ΔH1-ΔH2)
(3ΔH3-ΔH1-ΔH2)
C.ΔH4= (ΔH1+ΔH2-3ΔH3)
(ΔH1+ΔH2-3ΔH3)
D.ΔH4= (ΔH1-ΔH2-3ΔH3)
(ΔH1-ΔH2-3ΔH3)
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.含有NA个氦原子的氦气在标准状况下的体积约为11.2 L
B.25℃,1.01×105 Pa,64 g SO2中含有的原子数为3NA
C.在常温常压下,11.2 L Cl2含有的分子数为0.5 NA
D.标准状况下,11.2 L H2O含有的分子数为0.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
为了除去氯化钠样品中的杂质碳酸钠,某兴趣小组最初设计了如下方案并进行了实验。

(1)写出沉淀A的化学式___________________________;
(2)加入过量氯化钙溶液后,分离除去沉淀A的实验操作方法是____________________
_______________________________________________________________________。
(3)他们在实验过程中,又发现了新的问题:此方案很容易引入新的杂质,请写出固体物质B的成分________(用化学式表示);
(4)他们继续探究后又提出了新的方案:将混合物溶解,滴加盐酸至不再产生气体为止,既能除去碳酸钠杂质,又能有效地防止新杂质的引入。有关反应的化学方程式为
___________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com