
| A.1︰9 | B.9︰1 | C.1︰11 | D.11︰1 |


 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源:不详 题型:单选题
| A.C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l) ΔH= -a kJ?mol-1 |
| B.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH= -b kJ?mol-1 |
| C.2CO(g)+O2(g)=2CO2(g) ΔH= -c kJ?mol-1 |
| D.NH3(g)+5/4O2(g)=NO(g)+6/4H2O(g) ΔH= -d kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
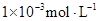 的氨水
的氨水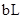 ②
②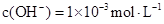 的氨水cL
的氨水cL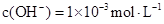 的
的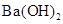 的溶液
的溶液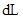
A.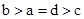 | B.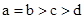 | C.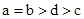 | D.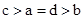 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
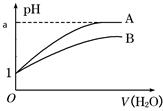
| A.A酸比B酸的电离程度小 |
| B.A是强酸,B是弱酸 |
| C.pH=1时,B酸的物质的量浓度比A酸大 |
| D.将pH=1的A酸和B酸稀释成pH=5的溶液,A酸所需加入的水量多 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.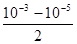 mol·L-1 mol·L-1 | B.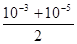 mol·L-1 mol·L-1 |
C. mol·L-1 mol·L-1 | D.以上计算式都不对 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(CH3COO-)=c(Na+)时,该溶液一定呈中性 |
| B.c(CH3COO-)=c(Na+)时,醋酸和氢氧化钠恰好完全中和 |
| C.c(CH3COO-)>c(Na+)>c(H+)>c(OH-)时,可能是醋酸过量 |
| D.c(Na+)>c(CH3COO-)>c(OH-)>c(H+)时,一定是NaOH过量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.a的浓度必小于乙酸的浓度 | B.a的浓度必大于乙酸的浓度 |
| C.b的浓度必小于乙酸的浓度 | D.b的浓度与乙酸的浓度无法比较 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com