
| A、4:9 | B、1:1 |
| C、7:6 | D、4:3 |
| 14g |
| 28g/mol |
| 12g |
| 32g/mol |


科目:高中化学 来源: 题型:
| A、N2既是氧化产物又是还原产物 |
| B、氧化产物与还原产物物质的量之比为1:2 |
| C、联氨是氧化剂 |
| D、氧化剂与还原剂物质的量之比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、O2和O3的混合气体共6.4g,其中所含氧原子数一定为0.4NA |
| B、常温常压下,22.4L二氧化碳含有的原子总数为3NA |
| C、将标准状况下22.4L NO与11.2L O2混合后所含分子数为1.5NA |
| D、物质的量浓度为0.25mol?L-1的MgCl2溶液中含有Cl个数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
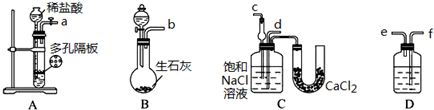
| 氨碱法 | 联合制碱法 | ||
| A | 原料 | 食盐、氨气、生石灰 | 食盐、氨气、二氧化碳 |
| B | 可能的副产物 | 氯化钙 | 氯化铵 |
| C | 循环物质 | 氨气、二氧化碳 | 氯化钠 |
| D | 评价 | 原料易得;设备复杂;能耗高 | 原料利用率高;废弃物少 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、联合制碱法生产的两种产品一种是碱,一种是盐 |
| B、在硫酸工业生产过程的接触室中运用热交换技术可充分利用能源 |
| C、在合成氨生产中有原料循环使用的工艺,可以提高原料的利用率 |
| D、用烧碱溶液吸收精制硝酸产生的尾气中的氮氧化物符合绿色化学理念 |
查看答案和解析>>
科目:高中化学 来源: 题型:

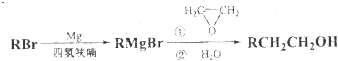
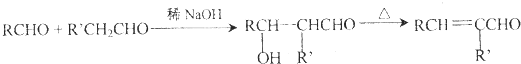
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石油裂解、煤的气化、海水制镁都包含化学变化来源 |
| B、福尔马林可制备标本是利用了使蛋白质变性的性质 |
| C、含钙、钡、铂等金属元素的物质有绚丽的颜色,可用于制造焰火 |
| D、红葡萄酒储藏时间长后变香可能是因为乙醇发生了酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
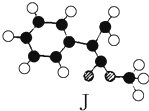 肉桂酸甲酯(H)是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精.它的分子式为C10H10O2,且分子中只含有1个苯环,苯环上只有一个取代基.又知J为肉桂酸甲酯的一种同分异构体,其分子结构模型如图所示(图中球与球之间连线表示单键或双键).
肉桂酸甲酯(H)是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精.它的分子式为C10H10O2,且分子中只含有1个苯环,苯环上只有一个取代基.又知J为肉桂酸甲酯的一种同分异构体,其分子结构模型如图所示(图中球与球之间连线表示单键或双键).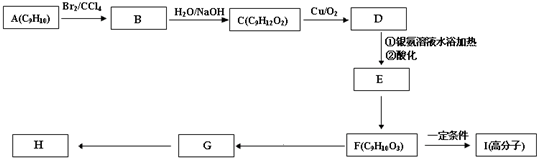
查看答案和解析>>
科目:高中化学 来源: 题型:
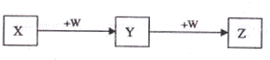
| A、若W是单质铁,则Z溶液可能是FeCl2溶液 |
| B、若W是氢氧化钠,则X水溶液呈酸性 |
| C、若W是氧气,则X、Z的相对分子质量可能相差48 |
| D、若W是强氧化性的单质,则X可能是金属铝 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com