
【题目】有关物质的转化关系如下图所示。A、B、C、E为气体,其中A能使湿润的红色石蕊试纸变蓝,B为无色单质,E是为红棕色。G是紫红色金属单质,H的水溶液为蓝色。
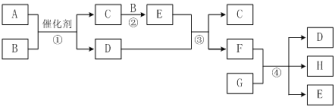
⑴A的电子式为______。
⑵写出反应①的化学方程式:______。
⑶写出反应③的化学方程式:______。该方程式中转移的电子数目为______个。
⑷写出反应④的离子方程式:_____。
【答案】![]() 4NH3+5O2
4NH3+5O2 ![]() 4NO+6H2O 3NO2+H2O=2HNO3+NO 2 4H++2NO3-+Cu=2NO2↑+2H2O+Cu2+
4NO+6H2O 3NO2+H2O=2HNO3+NO 2 4H++2NO3-+Cu=2NO2↑+2H2O+Cu2+
【解析】
A、B、C、E为气体,其中A能使湿润的红色石蕊试纸变蓝,则气体A是碱性气体,则A为NH3;E是为红棕色气体,则E为NO2;根据物质转化关系,NH3和B在催化剂条件下反应生成C和D,C和B反应生成NO2,则该反应为氨气的催化氧化反应,因此C为NO,B为O2,D为H2O;NO2(E)和H2O(D)反应生成NO和HNO3,则F为HNO3;G是紫红色金属单质,则G为Cu;HNO3和Cu反应生成NO、Cu(NO3)2和H2O,H的水溶液为蓝色,则H为Cu(NO3)2。
⑴根据分析,A为NH3,电子式为![]() 。
。
答案为:![]() 。
。
(2)反应①为氨气和氧气在催化剂条件下发生催化氧化反应,化学方程式4NH3+5O2 ![]() 4NO+6H2O。
4NO+6H2O。
答案为:4NH3+5O2 ![]() 4NO+6H2O。
4NO+6H2O。
⑶反应③为NO2和H2O反应生成NO和HNO3,化学方程式:3NO2+H2O=2HNO3+NO。该方程式中3个NO2参与反应,2个NO2从+4价升高到+5价,1个NO2从+4价降低到+2价,共转移电子2个。
答案为:2。
⑷反应④为HNO3和Cu反应生成NO、Cu(NO3)2和H2O,离子方程式:4H++2NO3-+Cu=2NO2↑+2H2O+Cu2+。
答案为:4H++2NO3-+Cu=2NO2↑+2H2O+Cu2+。


 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:
【题目】关于实验室中四个装置的说明符合实验要求的是
A. 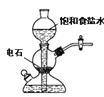 若需制备较多量的乙炔可用此装置
若需制备较多量的乙炔可用此装置
B.  可用此装置来制备硝基苯,但产物中可能会混有NO2
可用此装置来制备硝基苯,但产物中可能会混有NO2
C.  可用此装置来分离含碘的四氯化碳液体,最终在锥型瓶中可获得碘
可用此装置来分离含碘的四氯化碳液体,最终在锥型瓶中可获得碘
D.  可用此装置来制备乙酸乙酯并在烧瓶中获得产物
可用此装置来制备乙酸乙酯并在烧瓶中获得产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤族元素包括氯、溴、碘等元素,其中溴和碘在陆地上含量极少,主要存在于海水中。
(1)氯气有毒,一旦泄露会造成对空气的严重污染。工业上常用浓氨水检验氯气管是否漏气。(已知Cl2可将NH3氧化成N2)写出有关的化学方程式_________________________________。
(2)亚氯酸钠(NaClO2)是一种漂白剂。 已知NaClO2变质可分解为NaClO3和NaCl。取等质量变质前后的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量相同,从电子守恒的角度解释其原因是_________________________________________。
(3)从海水中提取溴,一般要经过浓缩、氧化和提取三个步骤。氧化时常用氯气做氧化剂,写出有关的离子方程式___________________________________________________________。海带提碘时,由于碘的量较少,在灼烧、溶解之后得到的溶液用硝酸银溶液很难检验。设计一个检验溶液中是否含有碘离子的方法_________________________________________。
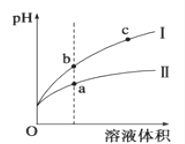
(4)盐酸和醋酿都是一元酸,某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,平衡pH随溶液体积变化的曲线如下图所示。据图判断盐酸稀释时的pH变化曲线为___________ (填“I”或“II”),溶液的导电性b ___________ c(填“>”、“<”或“=”)。水电离的c(H+)a点比b点大还是小?从电离平衡移动原理解释原因________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,下列溶液的离子浓度关系式正确的是
A. pH=5的H2S溶液中,c(H+)= c(HS-)=1×10—5mol·L—1
B. pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C. pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+ c(H+)= c(OH-)+c( HC2O4-)
D. pH相同的①CH3COO Na②NaHCO3③NaClO三种溶液的c(Na+):①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在体积为5 L的密闭容器中发生可逆反应。(Ⅰ)若某可逆反应的化学平衡常数表达式为:K=![]()
(1)写出该反应的化学方程式:
(2)能判断该反应一定达到化学平衡状态的依据是 (填选项编号)。
A.容器中气体的平均相对分子质量不随时间而变化
B.v正(H2O)=v逆(H2)
C.容器中气体的密度不随时间而变化
D.容器中总质量不随时间而变化
E.消耗n mol H2的同时消耗n mol CO
(Ⅱ)若该密闭容器中加入的是2 mol Fe(s)与1 mol H2O(g),t1秒时,H2的物质的量为0.20 mol,到第t2秒时恰好达到平衡,此时H2的物质的量为0.35 mol。
(1)t1~t2这段时间内的化学反应速率v(H2)= 。
(2)若继续加入2 mol Fe(s),则平衡 移动(填“向正反应方向”、“向逆反应方向”或“不”),继续通入1 mol H2O(g),再次达到平衡后,H2物质的量为 mol。
(3)该反应的逆反应速率随时间变化的关系如图。t1时改变了某种条件,改变的条件可能是 、 (填写2项)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品。现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物,下列框图是分离操作步骤流程图:

则试剂a是________,分离方法Ⅰ是________,分离方法Ⅱ是________,试剂b是________,分离方法Ⅲ是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,同时也是对烟气进行脱硫、脱硝的吸收剂。其一种生产工艺如下:
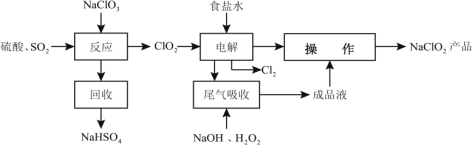
已知:
纯ClO2易分解爆炸,空气中 ClO2的体积分数在 10%以下比较安全;
NaClO2在碱性溶液中稳定存在,在酸性溶液中迅速分解;
NaClO2饱和溶液在温度低于 38℃时析出 NaClO23H2O,等于或高于38℃时析出 NaClO2,高于 60℃时分解成 NaClO3和 NaCl。回答下列问题:
(1)写出“反应”步骤中生成 ClO2的化学方程式_________。
(2)从滤液中得到的 NaClO23H2O 晶体的方法是_________。
(3)“尾气吸收”是吸收“电解”过程排出的少量 ClO2 。在尾气吸收过程中,可代替 H2O2的试剂是_________(填序号)。
A.Na2O2 B.Na2S C.FeCl2 D.KMnO4
(4)国家标准规定产品中优级纯试剂纯度≥99.8%,分析纯试剂纯度≥99.7%,化学纯试剂纯度≥99.5%。为了确定某批次 NaClO2产品的等级,研究小组设计测定方案如下:取 10.00g 样品,用适量蒸馏水溶解后,加入略过量的 KI 溶液;充分反应后,将反应液定容至 200mL, 取出 20.00mL 于锥形瓶;向锥形瓶中滴加两滴淀粉溶液,用 2.00molL﹣1的 Na2S2O3溶液与之反应,消耗Na2S2O3溶液 22.00mL。该样品可达试剂纯度 ________________。(写出计算过程) 已知: ClO2﹣+4I﹣+4H+═2H2O+2I2+Cl﹣ , I2+2S2O32﹣═2I﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com