
分析 (1)设NO和NO2的物质的量分别为xmol、ymol,根据二者总体积、电子转移守恒列方程,再根据V=nVm体积.
(2)根据N原子守恒计算消耗的硝酸.
解答 解:(1)32.64g铜的物质的量为$\frac{32.64g}{64g/mol}$=0.51mol,在反应中失去的电子的物质的量为2×0.51mol=1.02mol,11.2L混合气体的物质的量为$\frac{11.2L}{22.4L/mol}$=0.5mol
令NO和NO2的物质的量分别为xmol、ymol,则:$\left\{\begin{array}{l}{x+y=0.5}\\{3x+y=1.02}\end{array}\right.$
解得x=0.26,y=0.24,
V(NO)=0.26mol×22.4L/mol=5.824L;
答:NO的体积为5.824L;
(2)由N原子守恒可知,反应消耗的硝酸为n(HNO3)=2n(Cu(NO3)2)+n(NOx)=0.51mol×2+0.5mol=1.52mol;
答:消耗的硝酸物质的量为1.52mol.
点评 本题考查化学方程式计算,难度不大,注意利用电子转移守恒和原子守恒进行解答,避免利用方程式计算的繁琐,侧重于考查学生的分析能力和计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | Al(OH)3是医用的胃酸中和剂的一种 | |
| B. | 铁的氧化物都不溶于水,但可与水反应 | |
| C. | 铁容易形成致密的氧化膜,抗腐蚀性能好 | |
| D. | 取一片铝条放在酒精灯上加热至熔化,铝会滴落下来 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | MgSO4的溶解度随温度升高而升高 | |
| B. | NaCl的溶解度比MgSO4的溶解度大 | |
| C. | 在t2℃时,MgSO4饱和溶液的溶质质量分数最大 | |
| D. | 把MgSO4饱和溶液的温度从t3℃降至t2℃时,有晶体析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
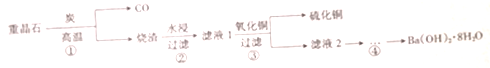
| A. | 步骤①中BaSO4作氧化剂 | |
| B. | 步骤②所得滤液1呈中性 | |
| C. | 步骤③中发生复分解反应 | |
| D. | 步骤④的实验操作中不需要用到石棉网、坩埚 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:r(C)<r(D)<r(B) | |
| B. | 元素A与B只能形成一种化合物 | |
| C. | A的简单气态氢化物的热稳定性比C的强 | |
| D. | C的最高价氧化物的水化物的酸性比D的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol对苯二甲酸中含有双键的数目为0.2NA | |
| B. | 常温下,1L pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA | |
| C. | Fe在少量Cl2中燃烧生成0.5 mol产物,转移的电子数为NA | |
| D. | 标准状况下,2.24L H2S全部溶于水所得溶液中HS-和S2-离子数之和为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com