
| A、AlCl3溶液 |
| B、AgNO3溶液 |
| C、Na2SO4溶液 |
| D、NaOH溶液 |
| ||
| ||
| ||
| ||


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、Na2SO3溶液(BaCl2溶液) |
| B、FeCl2溶液(KSCN溶液) |
| C、KI溶液(淀粉溶液) |
| D、氯水(品红溶液) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
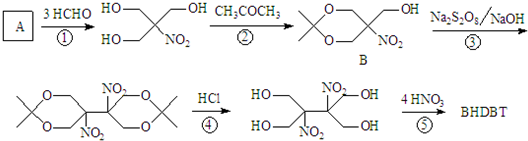
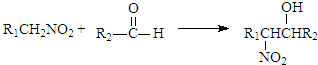 (将R1CH2NO2中硝基换为醛基,也能发生类似反应)
(将R1CH2NO2中硝基换为醛基,也能发生类似反应)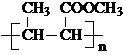 ),合成过程中无机试剂任选,合成路线流程图示例如下:CH3CH2OH
),合成过程中无机试剂任选,合成路线流程图示例如下:CH3CH2OH| 浓硫酸 |
| 170℃ |
| Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
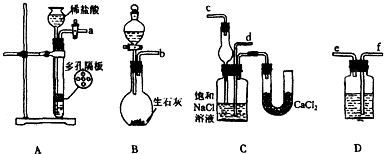
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浓硫酸具有吸水性,因而能使蔗糖炭化 |
| B、浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 |
| C、常温下,金属铁遇浓硫酸时会在表面生成致密的氧化膜而发生钝化 |
| D、50mL 18mol?L-1硫酸中加入足量的铜粉反应放出二氧化硫气体少于10.08L |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用过量氨水除去Al3+溶液中的少量Fe3+ |
| B、将混合气体通过灼热的铜网除去N2中的少量O2 |
| C、向某溶液中加HCl酸化的BaCl2溶液,产生白色沉淀,则该溶液中一定含有SO42- |
| D、向澄清石灰水中通入少量气体产生沉淀,过量时沉淀溶解,说明该气体一定是CO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com